Большая Энциклопедия Нефти и Газа. Замерзание воды это явление
«обыкновенные чудеса» в нашей жизни
Вода – самое распространенное и самое загадочное вещество на нашей планете. Она обладает простыми свойствами, известными с древних времен. Именно благодаря этим особенностям ее и называют «основой жизни». Так в чем же «чудесность» этих свойств? Давайте разбираться.
Текучесть. Основное свойство всех жидкостей, и воды – в том числе. Под действием внешних сил она способна принимать форму любого сосуда. И это обеспечивает ее повсеместную доступность. Вода течет в водопроводах, образует озера, реки и моря. И, самое главное, вы всегда можете взять ее с собой в любой удобной упаковке – от маленькой бутылочки до огромной цистерны.
Температурные свойства. Теплая вода легче холодной и всегда поднимается вверх. Поэтому мы можем готовить суп, нагревая кастрюлю только снизу, а не со всех сторон сразу. Благодаря этому явлению, называемому «конвекцией», большинство обитателей земных водоемов живут ближе к поверхности.
Но самым важным из температурных свойств воды является ее высокая теплоемкость – в 10 раз больше, чем у железа. Это значит, что для ее нагревания необходимо большое количество энергии, однако и при остывании энергии выделяется столько же. На этом принципе основаны системы отопления в наших домах – и системы охлаждения, применяемые в промышленности.
Кроме того, моря и океаны играют роль терморегулятора Земли, смягчая сезонные перепады температуры, поглощая тепло летом и отдавая его зимой. А при сочетании теплоемкости и конвекции можно даже обогреть целый континент! Речь идет о «главной батарее Европы», теплом течении Гольфстрим. Гигантские потоки теплой воды, двигаясь по поверхности Атлантики, обеспечивают на ее побережье комфортную температуру, не свойственную для этих широт.
Замерзание.Температура замерзания воды условно равна 0 градусов, но на самом деле этот параметр зависит от ряда факторов: атмосферного давления, емкости, в которую вода помещена, от наличия в ней примесей.
Вода уникальна тем, что, в отличие от других веществ, при замерзании расширяется. При наших суровых зимах, это, пожалуй, можно назвать отрицательным свойством. Замерзая и увеличиваясь в объеме, вода (а точнее, уже лед) просто рвет трубы из металла.
Итак, при переходе в твердое состояние вода увеличивается в объеме, но становится не такой плотной. Поэтому лед всегда легче воды, и находится на ее поверхности. К тому же, он плохо проводит тепло: даже самой холодной зимой в водоемах планеты сохраняется жизнь. Ведь чем толще ледяная «подушка», тем теплее вода под ней. Также, благодаря этому свойству, некоторые народы до сих пор строят так называемые «ледники» – погреба или пещеры, обложенные льдом, который не тает даже летом, и позволяет хранить продукты очень долго.
Некоторые ученые даже предложили использовать лед в борьбе с глобальным потеплением. Суть идеи такова – специальный корабль берет на буксир айсберг, дрейфующий где-нибудь близ Антарктиды. А потом тащит его в теплые края, где люди страдают от жары. Айсберг тает, обеспечивая прохладой целый прибрежный регион. Такой вот «Гольфстрим наоборот», только созданный человеком.
Закипание. От холодного льда перейдем к горячему пару. Всем известно, что вода закипает при температуре в 100 градусов Цельсия. Но это лишь в условиях нормального состава воздуха и атмосферного давления. Зато на вершине Эвереста, где давление ниже, а воздух разрежен, ваш чайник закипит уже при 68 градусах! Кипячение воды способствует тому, что в ней погибают вредные микроорганизмы. А еще продукты, приготовленные на пару, намного более полезны, чем жареные.
К тому же, водяной пар можно назвать настоящим двигателем цивилизации. Еще не прошло и ста лет с эпохи паровых двигателей, и многие до сих пор ошибочно называют железнодорожные локомотивы (работающие сейчас преимущественно на электричестве) «паровозами».
Кстати, об электричестве. Без пара оно до сих пор оставалось бы редкой и дорогой диковинкой. Ведь принцип работы большинства электростанций основан на вращении ротора под давлением горячего пара. Современные атомные станции отличаются от старых угольных или нефтяных только принципом нагрева воды. Даже инновационная и безопасная солнечная энергетика использует пар: огромные зеркала, подобно лупе, фокусируют солнечные лучи на резервуаре с водой, превращая ее в пар для электротурбин.
Растворение. Еще одно важнейшее свойство воды, без которого была бы невозможна не только наука и промышленность, но и сама жизнь! Как думаете, что общего между плазмой крови и вашей любимой газировкой? Ответ прост: газировка – это водный раствор различных солей, минералов и газов. Плазма же состоит на 90% из воды, а также из белков и других веществ. И каждая клетка живого организма получает нужные ей вещества тоже в виде водного раствора.
Вода является самым простым, безопасным, но, тем не менее, самым надежным природным растворителем. Между ее подвижных молекул могут «затесаться» практически любые вещества – от жидкостей до металлов. Это чудесное свойство было замечено еще на заре человечества. Древние художники растворяли в воде природные красители, чтобы рисовать на стенах пещер. Потом эстафету приняли средневековые алхимики, растворяя в воде самые разные вещества в надежде получить «философский камень», превращающий любой материал в золото. А теперь это свойство с успехом используют современные химики.
Поверхностное натяжение. Большинство людей, слыша про поверхностное натяжение воды, вспоминают разве что насекомых-водомерок, скользящих по глади пруда или лужи. А, между тем, без этого свойства воды невозможно даже вымыть руки! Именно благодаря ему образуется мыльная пена. Да и вытереть руки полотенцем без него тоже сложно. Ведь все впитывающие материалы (неважно, бумажная салфетка или ткань из микрофибры) обладают микроскопическими порами, в которые влага впитывается за счет поверхностного натяжения. По этой же причине вода устремляется по тончайшим капиллярам, пронизывающим корни растений. И приготовление сухих строительных смесей также возможно благодаря поверхностному натяжению добавляемой воды.
Молекулы воды активно притягиваются друг к другу, в результате ее поверхность при данном объеме стремится к минимиму. Именно поэтому естественной формой любой жидкости является шар. Это легко можно проверить оказавшись в невесомости. Хотя, для подобного эксперимента не обязательно лететь в космос, просто введите с помощью шприца немного воды в стакан с растительным маслом и наблюдайте, как она соберется в шарики.
Фото: Shutterstock, NASA.
www.da-voda.com
Феномен замерзающей воды
Любой владелец дачного домика для сезонного проживания знает, что необходимо в обязательном порядке слить воду из летнего водопровода до прихода устойчивых морозов. Замерзшая вода повредит трубы, сведя на нет все усилия по обустройству автономной системы водоснабжения, на которое было затрачено много средств. Копка колодца или бурение скважины на воду, прокладка труб и организация водопровода в доме, как известно, требуют значительных капитальных вложений.
Но процесс замерзания воды, кроме негативных последствий, обладает еще и качеством, которым интересуются даже представители ученых кругов. Это парадоксальная способность горячей воды замерзать быстрее, чем холодной.
Открытие эффекта Мпембы
Впервые эффект ускоренного замерзания жидкости был замечен простым учеником простой школы в Танзании. Эрасто Мпемба обратил внимание на то, что при приготовлении мороженого горячая молочная смесь, поставленная в морозильную камеру, застывает за менее короткий промежуток времени, чем такая же смесь, но предварительно охлажденная. Выяснил он это случайным образом, но, заинтересовавшись явлением, начал проводить опыты уже с водой.
Нужно отметить, что с феноменом ускоренного замерзания кипятка были знакомы такие известные личности, как Рене Декарт и Аристотель, но вплотную им занялся именно школьник из Танзании, и произошло это только в середине XX века. Своими исследованиями он поделился с университетским профессором Денисом Осборном. Тот азартно принялся за проведение экспериментов, пригласив в компанию любознательного Мпембу. Результаты опытов позднее были опубликованы в одном из научных журналов, а само свойство воды получили название «эффект Мпембы».
Как ученые объясняют феномен Мпембы
После проведение огромного количества опытов с водой, создавая различные условия, при которых наблюдалось образование льда, ученые сделали вывод, что эффект Мпембы могут вызывать разные факторы. Вот некоторые из них…
Парообразование
Испаряясь, горячая вода начинает терять свой объем, кроме того, процесс испарения сопровождается понижением температуры испаряющейся жидкости. Как следствие, процесс замерзания идет интенсивнее и начинается быстрее, чем у сравнительного образца — емкости с холодной водой.
Температура воды
Большой разрыв между уровнями температуры воды и охлаждающей среды обуславливает увеличенную интенсивность теплообмена, что влечет за собой быстрое охлаждении жидкости.
Эффект переохлаждения
Известно, что процесс полного замерзания переохлажденной жидкости идет за менее короткий срок, чем постепенное образование кристаллов льда. Переохлаждение связано с отсутствием центра кристаллизации, в роли которого могут выступать пузырьки газов. В горячей воде минимальное количество растворенных газов, так как в процессе кипения они в большинстве своем выделились в окружающую среду. Но всегда наступает критический момент, когда в переохлажденной воде начинается образовываться лед, но за счет слишком низкой температуры воды, интенсивность возникновения кристаллов льда значительно возрастает.
Кроме перечисленных факторов, ученые упоминают также конвенцию, теплопроводность, различные химические примеси и прочее. Существуют даже формулы, доказывающие существование эффекта Мпембы. Но при этом парадокс так и остается парадоксом, а ученые пока не пришли к единой версии его объяснения.
spb-burenie.ru
При какой температуре замерзает вода?
В моем детстве в магазинах мало чего было, а летом в жару очень хотелось мороженого. Я, как и многие советские детишки, в морозильной камере замораживал воду с разведенным вареньем, то и дело заглядывал, готово ли.
Еще тогда изучил, что лед получается при температуре ниже 0 градусов. Став старше, узнал, как проходит процесс замерзания, какая температура нужна для этого разным водным растворам.
При какой температуре замерзает вода
Вода – это самая загадочная субстанция на планете. Она бывает разной:
- пресной и питьевой;
- минеральной;
- морской и солоноватой;
- дистиллированной и деионизированной.
От ее состава как раз и зависит температура замерзания. Обычная питьевая вода превращается в лед при температуре 0 градусов по Цельсию.
Но если добавить в нее различные соли, сахар или спирт, тогда потребуется температура значительно ниже. Дистиллированная вода, в которой отсутствуют примеси, и вовсе замерзает, если охладить ее ниже -42 градусов, в обычном холодильнике такой опыт не получится. При давлении даже простая водопроводная вода начнет замерзать только при отметке -2 градуса, чем больше оно будет, тем ниже потребуется температура. Чтобы понять, отчего так происходит, надо поближе познакомиться с процессом замерзания.
Как замерзает вода
В обыкновенной воде есть микроскопические частички, это может быть пыль, глина, песок. При понижении температуры и достижении отметки в 0 градусов они становятся центрами, вокруг которых появляются кристаллы льда. Пузырьки воздуха, трещины на посуде тоже могут стать такими ядрами кристаллизации. Чем их больше, тем быстрее пойдет процесс.
Для воды с примесью соли и прочих добавок требуется больше времени для замерзания потому, что у нее высокая плотность, и чем она выше, тем дольше жидкость будет замерзать. Дистиллированную воду вообще невозможно заморозить в домашних условиях из-за отсутствия таких центров, если в ней нет пузырьков воздуха и трещинок на емкости, в которую она налита.
Может ли вода замерзнуть при положительной температуре
Мне известны 2 фактора, при которых лед образуется при плюсовых показателях температуры. На высоте более 1000 км вода начинает замерзать уже при температуре +2 градуса.
И совсем уж предстает загадочная картина, если в нее добавить каустическую соду. Чем выше концентрация, тем выше температура замерзания. Например, 44% раствор превратится в лед при температуре +7 градусов.
travelask.ru
Объяснение эффекта Мпембы расширением воды при замерзании : Помогите решить / разобраться (Ф)
Как Вы считаете, правильно ли нижеследующее объяснение эффекта Мпембы?
Прежде, чем рассматривать так называемый «эффект Мпембы», как физическое явление, и пытаться что-то объяснить, неплохо бы определиться с тем, что и при каких условиях наблюдаем, и есть ли вообще эффект. Вы вот, например, пишете о воде (дистиллированной?), но пресловутый Мпемба, насколько мне известно, замораживал вовсе не воду, а пытался приготовить мороженое. Более того, ни в одной научной или околонаучной публикации я не встречал ни чёткого описания эффекта (что и при каких условиях замораживаем) ни, соответственно, двух похожих объяснений — каждый исследователь рассматривал что-то своё (причём многие «исследователи» сразу предлагают «объяснение», даже не пытаясь конкретизировать проблему или самостоятельно воспроизвести «эффект»). Всё это больше напоминает «ловлю рыбки в мутной воде», а не научную работу.Несколько лет назад, после очередных дебатов в каком-то форуме, я лично поставил следующий опыт. Зимой на даче, взял два одинаковых стеклянных стакана. В первый стакан налил из чайника кипячёную воду комнатной температуры (около 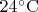 ) — примерно
) — примерно 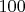 мл (вода родниковая, не минерализованная). После этого оставшуюся в чайнике воду довёл до кипения и налил такой же объём во второй стакан. Оба стакана тут же выставил на улицу на сухое деревянное крыльцо. Температура воздуха на крыльце была около
мл (вода родниковая, не минерализованная). После этого оставшуюся в чайнике воду довёл до кипения и налил такой же объём во второй стакан. Оба стакана тут же выставил на улицу на сухое деревянное крыльцо. Температура воздуха на крыльце была около  . Как и ожидалось, когда в стакане с холодной водой уже образовалась плотная корка льда, горячая вода во втором стакане и не думала замерзать. До полного замерзания процесс не контролировал. Но, как я уже упоминал, ни в одном описании «эффекта» не было дано чётких пояснений, что значит «замерзает быстрее», идёт ли речь о времени начала кристаллизации, или же имеется ввиду кристаллизация всего объёма воды или что-то ещё.
. Как и ожидалось, когда в стакане с холодной водой уже образовалась плотная корка льда, горячая вода во втором стакане и не думала замерзать. До полного замерзания процесс не контролировал. Но, как я уже упоминал, ни в одном описании «эффекта» не было дано чётких пояснений, что значит «замерзает быстрее», идёт ли речь о времени начала кристаллизации, или же имеется ввиду кристаллизация всего объёма воды или что-то ещё.
Это обеспечивает замерзание содержимого ледяной капсулы при более высокой температуре и образование большего количества льда за то же время для изначально более тёплой воды.
Предположим, первое утверждение верно (вопрос, верно ли оно на самом деле, оставим пока в стороне). Но каким образом это приведёт к более быстрому замерзанию горячей воды? Практика показывает, что при н.у. замерзание воды и образование ледяной корки начинается, когда температура поверхности воды достигнет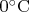 . В то время, как сосуд с холодной водой уже покроется ледяной коркой (и образуется упомянутая Вами «ледяная капсула»), в сосуде с изначально горячей водой ещё и не начнётся никаких процессов кристаллизации. Отталкиваясь от Ваших рассуждений, как раз в сосуде с холодной водой, где «капсула» образовалась раньше, и замерзание всего объёма должно завершиться раньше. «Капсула» приведёт лишь к более быстрому замерзанию — в лёд начнёт превращаться и тот объём воды, который ещё имеет температуру выше нуля (в то же время в стакане с горячей водой температура всё ещё высока и «капсулы» нет).
. В то время, как сосуд с холодной водой уже покроется ледяной коркой (и образуется упомянутая Вами «ледяная капсула»), в сосуде с изначально горячей водой ещё и не начнётся никаких процессов кристаллизации. Отталкиваясь от Ваших рассуждений, как раз в сосуде с холодной водой, где «капсула» образовалась раньше, и замерзание всего объёма должно завершиться раньше. «Капсула» приведёт лишь к более быстрому замерзанию — в лёд начнёт превращаться и тот объём воды, который ещё имеет температуру выше нуля (в то же время в стакане с горячей водой температура всё ещё высока и «капсулы» нет).Почему я считаю, что это объяснение может считаться истинным без проведения физических экспериментов? Это основано на следующем рассуждении.
Уважаемый Akymak! Времена схоластики в духе Аристотеля давно прошли. Так что лет 500-600 назад Ваше «считаться истинным без проведения физических экспериментов» может ещё и прокатило бы. Но сейчас физика — естественная наука, т.е. наука об окружающем нас мире, а не пустое словоблудие. Поэтому важнейшим критерием правильности объяснения является его соответствие эксперименту.Только для воды наблюдается эффект Мпембы.
С чего Вы взяли? Ещё раз повторю: первооткрыватель «эффекта» Мпемба замораживал вовсе не воду.На самом деле в холодной воде образуются льдоподобные структуры, которые, тем не менее, мешают кристаллизации ледяных кристаллов из жидкой воды
Экспериментально показано, что гигантские надмолекулярные комплексы в жидкой воде существуют вплоть до температуры Ц и что их концентрация падает с температурой. Время установления равновесия в воде - 10-17 часов. http://www.nkj.ru/archive/articles/20017/Не берусь судить о справедливости Ваших утверждений, но мне не нравится сам ход рассуждений и отсутствие какого-либо обоснования.Во-первых, в указанной статье нет никакого упоминания о «льдоподобных структурах» в воде. Нет и ни слова о том, что гигантские надмолекулярные комплексы препятствуют кристаллизации воды. Во-вторых, 10-17 часов (в соответствии с упомянутой статьёй) — это не время «установления равновесия в воде» вообще, а время, по истечении которого «концентрация ионов
Ц и что их концентрация падает с температурой. Время установления равновесия в воде - 10-17 часов. http://www.nkj.ru/archive/articles/20017/Не берусь судить о справедливости Ваших утверждений, но мне не нравится сам ход рассуждений и отсутствие какого-либо обоснования.Во-первых, в указанной статье нет никакого упоминания о «льдоподобных структурах» в воде. Нет и ни слова о том, что гигантские надмолекулярные комплексы препятствуют кристаллизации воды. Во-вторых, 10-17 часов (в соответствии с упомянутой статьёй) — это не время «установления равновесия в воде» вообще, а время, по истечении которого «концентрация ионов  и
и 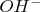 в воде принимает своё равновесное значение». А надмолекулярные комплексы в воде, надо полагать, образуются в достаточном количестве сразу же по мере снижения температуры, т.к. всё в той же статье их образование трактуется, как фазовые переходы, и связывается с определёнными характерными температурными точками воды:
в воде принимает своё равновесное значение». А надмолекулярные комплексы в воде, надо полагать, образуются в достаточном количестве сразу же по мере снижения температуры, т.к. всё в той же статье их образование трактуется, как фазовые переходы, и связывается с определёнными характерными температурными точками воды: Цитата:
Наиболее значимые соответствуют — температуре минимальной теплоёмкости,
— температуре минимальной теплоёмкости,  — температуре минимальной сжимаемости, и особенно характерен пик при
— температуре минимальной сжимаемости, и особенно характерен пик при 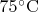 — температуре максимальной скорости звука в воде. Их можно трактовать как своеобразные фазовые переходы, связанные с разрушением эмулонов. При этом нет никаких упоминаний о том, что максимальная скорость звука в воде или минимальная теплоёмкость наблюдаются не сразу после достижения водой указанной температуры, а только через несколько часов и вообще как-то связаны с предысторией воды, а не с одной лишь температурой.
— температуре максимальной скорости звука в воде. Их можно трактовать как своеобразные фазовые переходы, связанные с разрушением эмулонов. При этом нет никаких упоминаний о том, что максимальная скорость звука в воде или минимальная теплоёмкость наблюдаются не сразу после достижения водой указанной температуры, а только через несколько часов и вообще как-то связаны с предысторией воды, а не с одной лишь температурой.dxdy.ru
зимой озеро замерзает. при замерзании воды...
Замерзание (физич. географ. и метеорол. ) — Физики и химики исследуют переход самых разнообразных тел из жидкого в твердое состояние при очень различных температурах. имеет значение лишь вода (с водяными растворами солей) , как тело очень распространенное на земном шаре и переходящее в твердое состояние при давлениях и температурах, встречаемых в земной атмосфере, водах и земной коре. В большей части источников, рек, проточных озер и отчасти и в земной коре вода встречается хотя и не в чистом виде, но с примесями столь малыми, что физические свойства этих вод, обыкновенно наз. пресными, существенно не отличаются от свойств чистой воды. Очень важно то, что вода замерзает при 0° и имеет наибольшую плотность около 4° Ц. Это значительно способствует З. пресных вод, стоячих или находящихся в слабом движении. При температурах выше 4° вода тем легче, чем теплее, а при температурах ниже 4°, обратно, — чем холоднее вода, тем она легче; холодная вода остается наверху и, следовательно, легко замерзает. Поэтому большие пресноводные озера (напр. Ладога, Онега, Байкал) , с лишком на 9/10 наполненные водой около 4°, могут замерзать сплошь зимою. Ветры, разводя волнение, замедляют сплошное замерзание; они разбивают лед — и перемешивают слои воды между собою, т. е. наиболее холодную верхнюю с более теплой нижележащей. Чем глубже водоем, тем больше волнение при той же силе ветра. Малые озера иногда в одну ночь замерзают сплошь, а оз. Байкал лишь 3 месяца после того, как средняя температура окружающего воздуха опустилась ниже 0°. На быстро текущих реках З. идет недружно и долго задерживается тем, что течение перемешивает слои воды и не дает верхнему слою остыть до 0°. На таких реках часто лед образуется не сверху (сало) , а сначала на дне, затем льдины всплывают, мелкие соединяются между собою и т. д. Это явление — образование придонного льда — не вполне еще разъяснено. Иные думают, что происходит охлаждение дна через лучеиспускание сквозь воду. Часто старались найти зависимость между временем З. рек, озер и т. д. и суммами средних суточных температур воздуха ниже 0° от начала морозов до дня З. (см. Рыкачева "Вскрытие и замерзание вод в России"), но очевидно, что точного соответствия быть не может: теплоемкость воздуха настолько мала сравнительно с теплоемкостью воды, что он оказывает заметное влияние главным образом на неглубокие водоемы и то при сильном ветре. Гораздо важнее для З. лучеиспускание поверхности воды. Поэтому при прочих равных условиях воды быстрее замерзают в ясную погоду, чем в пасмурную и туманную. Раз на водоеме образовался лед и в особенности после того, как он покрылся снегом, эти тела, как дурные проводники тепла, защищают воду от охлаждения, и дальнейшее З. ее идет медленнее. В воде морей и непроточных озер настолько много солей, что они значительно видоизменяют физические свойства воды.
да, безусловно.
Лёд образуется при температуре воздуха ниже нуля. Его толщина устанавливается, когда скорость образования льда снаружи равна скорости его подтапливания внизу. Когда температура воды в водоёме станет нулевой, подтапливание прекращается, и тогда толщина льда непрерыно растёт, пока держится отрицательная температура.
Но не все, т. к. существуют водородные связи и это ведет к аномалиям в строении и свойствах воды.
touch.otvet.mail.ru
Невероятная сила замёрзшей воды

Описание
В данном опыте, мы заполнили специальную железную ёмкость обычной водой (температура воды - 7-9 оС ). Сверху, ёмкость прикрыли подвижной крышкой специальной формы. Поверх крышечки мы поместили железный стрежень, который плотно прижали к крышке. Далее мы поместили нашу конструкцию в ёмкость, которую заполнили смесью льда и соли (это необходимо для того, чтобы понизить температуру в ёмкости).
Через некоторое время вода внутри железной ёмкости замёрзла. Образовавшийся лёд начал давить на крышечку, которая передала давление на железный стержень. В определённый момент это давление стало настолько велико, что стержень не выдержал и лопнул (переломился напополам).
Объяснение
Ни для кого не секрет, что все тела при нагревание расширяются, а при охлаждении сжимаются. Это явление называется тепловым расширением тел. Тепловое расширение тел может привести к деформации и даже разрушению целых домов, если при строительстве забыть о том, что летом дом будет расширятся, а зимой - сжиматься. Именно поэтому, при строительстве, стараются использовать материалы с одинаковыми показателями теплового расширения.
Тепловое расширение виновато ещё и в том, что тела обладают наибольшей плотностью в твёрдом состоянии и меньшей - в жидком. Это правило действует почти для всех веществ на земле. Но есть вещества, которые ведут себя наоборот - при нагревании сжимаются, а при охлаждении расширяются. Именно к таким вещества и относиться вода!
Наибольшую плотность, вода приобретает при температуры в 4 оС. Если продолжать охлаждать воду, то её плотность будет не расти, а падать, а сама вода начнёт увеличивать свой объём! Плотность льда составляет 9/10 от плотности воды, а это значит, что при замерзании объём воды увеличивается примерно на 1/10 от первоначального.
Замерзая, лёд способен нанести огромные разрушения на пути своего расширения. Трещины в трубах, зданиях и дорогах, разрывы труб - всё это последствия образования льда в ненужных местах (в трещинах зданий и дорог, и на стыках труб).
Это интересно
Именно благодаря аномальному свойству воды расширятся при понижении температуры, существует жизнь на нашей планете: лёд, являясь менее плотным и лёгким, чем вода всегда образовывается на поверхность водоёмов. В тоже время, на дне водоёмов даже в самый лютый мороз, сохраняется "плюсовая температура" (4 оС), так как вода при такой температуре обладает наибольшей плотностью. Это позволяет водоёмам не промерзать до дна и сохранять в себе жизнь в холодные зимние месяцы.
virtuallab.by
Процесс - замерзание - Большая Энциклопедия Нефти и Газа, статья, страница 2
Процесс - замерзание
Cтраница 2
V, § 6), дают возможность описать некоторые соотношения, относящиеся к процессам замерзания воды и водных растворов в различных условиях. [16]
В соответствии с климатическими условиями в СССР часто приходится сталкиваться в строительном деле с процессами замерзания воды или таяния льда. [17]
При солености большей 24 695 % о температура наибольшей плотности ниже температуры замерзания, поэтому процесс замерзания морской воды происходит иначе, чем пресной. При замерзании только часть солей переходит в лед, другая часть стекает в воду в виде солевого раствора, увеличивая соленость воды. При быстром замерзании морской воды образуется молодой морской лед, который содержит большой процент рассола, так как из-за быстрого процесса замерзания он не успевает вытесняться и остается внутри морского льда. При понижении температуры вода из рассола вымерзает, что увеличивает соленость оставшейся части рассола. Со временем рассол медленно стекает вниз, в результате чего старый лед более пресный, чем молодой. [18]
Для получения криогидратной температуры не следует применять сильного охлаждения; нужно стараться возможно дольше растянуть процесс замерзания эвтектической смеси. [20]
Из приведенных выше экспериментов следует, что между жидкостью и твердой фазой, образующейся в процессе замерзания слабых растворов, возникает некоторая разность потенциалов, зависящая как от особенностей растворенного вещества, так и от скорости кристаллизации. Для определения заряда, который может быть унесен при отрывании капли, нельзя, как указывалось выше, исходить из удельного заряда, разделяющегося при кристаллизации растворов. [21]
Формирование льда в водоемах и водотоках начинается одновременно с переохлаждением воды; существует три основных типа процессов замерзания водоемов. [22]
Физический смысл гистерезиса ( рис. 5.10) может быть раскрыт при анализе и сопоставлении некоторых результатов исследований процессов замерзания и оттаивания воды в грунтах, цементном геле и бетоне. [23]
С циклическим воздействием среды связано также морозное разрушение бетонных и железобетонных конструкций, когда механизм коррозии определяется процессами замерзания и оттаивания поровой жидкости бетона. [24]
Если веществом, осаждающимся из раствора, является чистый растворитель, а не растворенное вещество, процесс осаждения тождественен процессу замерзания. [25]
От явлений, связанных с давлением пара, оказалось возможным перейти к другой группе явлений, а именно к процессам замерзания растворов. Вант-Гофф показал, что понижение температуры замерзания для одного и того же вещества в различных растворителях ( при равных условиях) будет обратно пропорционально теплоте плавления растворителя. [26]
Для факультетов промышленного и гражданского строительства и для факультетов гидротехнического строительства необходимо значительно полнее рассмотреть вопросы, относящиеся к процессам замерзания различных форм связанной воды в природных условиях и при производстве зимних работ, а также физико-химические основы процессов твердения вяжущих и коррозии бетона. [27]
Процесс затвердевания1, о котором идет речь в аксиоме, не следует рассматривать как физический процесс, сходный с процессом замерзания и пр. [28]
Он полагает, что квазижидкая масса, состоящая из независимых длинных цепочечных молекул, способна превратиться в твердый кусок каучука в результате воображаемого процесса мгновенного замерзания; при этом каждая индивидуальная молекула остается неподвижной в том положении и при той конфигурации, какую ей удалось занять в момент замерзания. Распределение конфигураций цепи в этой похожей на жидкость массе одинаково с тем распределением, которое Кун в более ранней работе [ 34а ] вывел для нитеобразных молекул, находящихся в растворе. Согласно этому представлению, жидкий и твердый каучуки отличаются друг от друга тем, что в жидком состоянии каждая индивидуальная молекула свободно может изменять свою конфигурацию, тогда как в твердом состоянии эта конфигурация является фиксированной. Далее Кун постулирует, что когда твердый материал, как целое, растянут, то каждая молекула принимает новую фиксированную конфигурацию, причем каждый размер молекулы изменяется в той же пропорции, как и соответствующий размер в объеме материала в целом. [29]
Температура замерзания воды в строительном растворе или бетоне практически должна быть ниже температуры замерзания, соответствующей данной концентрации водного раствора взятой соли, поскольку процесс замерзания происходит и в мелких порах и капиллярах. Кроме того, по мере твердения раствора или бетона с добавкой солей концентрация их меняется ( стр. [30]
Страницы: 1 2 3
www.ngpedia.ru