Белки в химическом составе организма. В состав простых белков входят
какие элементы входят, определение, строение
Что такое белок и какие функции в организме он берет на себя. Какие элементы входят в его состав и в чем особенность этого вещества.
Белки – главный строительный материал в человеческом организме. Если рассматривать в целом, то эти вещества составляют пятую часть нашего тела. В природе известна группа подвидов – только в теле человека содержится пять миллионов разных вариантов. С его участием формируются клетки, считающиеся главной составляющей частью живых тканей организма. Какие элементы входят в состав белков и в чем особенность вещества?
Тонкости состава
Молекулы белка в теле человека отличаются строением и берут на себя определенные функции. Так, главным сократительным белком считается миозин, который формирует мускулатуру и гарантирует передвижение тела. Он обеспечивает работу кишечника и движение крови по сосудам человека. Не менее важное вещество в организме – креатин. Функция вещества состоит в защите кожи от негативных действий – лучевых, температурных, механических и прочих. Также креатин защищает от поступления микробов извне.
В состав белков входят аминокислоты. При этом первая из них открыта в начале XIX века, а весь аминокислотный состав известен ученым с 30-х годов прошлого века. Интересно, что из двух сотен аминокислот, которые открыты сегодня, только два десятка формируют миллионы различных по структуре белков.
Главное отличие структуры – в наличии радикалов, имеющих различную природу. Кроме того, аминокислоты часто классифицируются с учетом электрического заряда. Каждая из рассматриваемых составляющих имеет общие характеристики – способность вступать в реакцию со щелочами и кислотами, растворимость в воде и так далее. Почти все представители аминокислотной группы участвуют в метаболических процессах.
Рассматривая состав белков, стоит выделить две категории аминокислот – заменимые и незаменимые. Они отличаются между собой способностью синтезироваться в организме. Первые вырабатываются в органах, что гарантирует хотя бы частичное покрытие текущего дефицита, а вторые – поступают только с едой. Если количество любой из аминокислот снижается, то это приводит к нарушениям, а иногда и к гибели.
Белок, в котором присутствует полный аминокислотный набор, носит название «биологически полноценный». Такие вещества входят в состав животной пищи. Полезными исключениями считаются и некоторые представители растений – например, фасоль, горох и соя. Главный параметр, по которому судят о пользе продукта – биологическая ценность. Если в роли основы рассматривать молоко (100%), то для рыбы или мяса этот параметр будет равен 95, для риса – 58, хлеба (только ржаного) – 74 и так далее.
Незаменимые аминокислоты, входящие в состав белка, участвуют в синтезе новых клеток и ферментов, то есть они покрывают пластические нужды и применяются в роли главных источников энергии. В состав белков входят элементы, которые способны к превращениям, то есть процессам декарбоксилирования и переаминирования. В упомянутых выше реакциях участвуют две группы аминокислот (карбоксильная и аминная).


Наиболее ценным и полезным для организма считается яичный белок, структура и свойства которого идеально сбалансированы. Вот почему процентное содержание аминокислот в этом продукте почти всегда берется за основу при сравнении.
Выше упоминалось, что белки состоят из аминокислот, и главную роль играют независимые представители. Вот некоторые из них:
- Гистидин – элемент, который получен в 1911 году. Его функция направлена на нормализацию условно-рефректорной работы. Гистидин играет роль источника для образования гистамина – ключевого медиатора ЦНС, участвующего в передаче сигналов к разным участкам организма. Если остаток этой аминокислоты снижается ниже нормы, то подавляется выработка гемоглобина в костном мозге человека.
- Валин – вещество, открытое в 1879 году, но окончательно расшифрованное только через 27 лет. В случае его нехватки нарушается координация, кожные покровы становятся чувствительными к внешним раздражителям.
- Тирозин (1846 год). Белки состоят из многих аминокислот, но этот играет одну из ключевых функций. Именно тирозин считается главным предшественником следующих соединений – фенол, тирамин, щитовидная железа и прочих.
- Метионин синтезирован только к концу 20-х годов прошлого века. Вещество помогает в синтезе холина, защищает печень от чрезмерного образования жира, имеет липотропное действие. Доказано, что такие элементы играют ключевую роль в борьбе с атеросклерозом и в регулировании уровня холестерина. Химическая особенность метионина и в том, что он участвует в выработке адреналина, входит во взаимодействие с витамином В.
- Цистин – вещество, строение которого установлено только к 1903 году. Его функции направлены на участие в химических реакциях, обменных процессах метионина. Также цистин вступает в реакцию с серосодержащими веществами (ферментами).
- Триптофан – незаменимая аминокислота, что входит в состав белков. Ее удалось синтезировать к 1907 году. Вещество участвует в обмене белка, гарантирует оптимальный азотистый баланс в организме человека. Триптофан участвует в выработке сывороточных белков крови и гемоглобина.
- Лейцин – одна из наиболее «ранних» аминокислот, известная с начала XIX века. Ее действие направлено на помощь организму в росте. Нехватка элемента приводит к нарушению работы почек и щитовидки.
- Изолейцин – ключевой элемент, участвующий в азотистом балансе. Ученые открыли аминокислоту только в 1890 году.
- Фенилаланин синтезирован в начале 90-х годов XIX века. Вещество считается основой при формировании гормонов надпочечников и щитовидки. Дефицит элемента – главная причина гормональных сбоев.
- Лизин получен только в начале XX века. Нехватка вещества приводит к накоплению кальция в костных тканях, уменьшению объема мускулатуры в организме, развитию анемии и так далее.


Стоит выделить и химический состав белков. Это не удивительно, ведь рассматриваемые вещества относятся к химическим соединениям.
- углерод – 50-55%;
- кислород – 22-23%;
- азот – 16-17%;
- водород – 6-7%;
- сера – 0,4-2,5%.
Кроме перечисленных выше, в состав белков входят следующие элементы (в зависимости от типа):
- медь;
- железо;
- йод;
- фосфор;
- микро- и макровещества.
Химическое содержание различных белков отличается. Единственное исключение – азот, содержание которого всегда 16-17%. По этой причине уровень содержания вещества определяется именно по процентному содержанию азота. Процесс вычисления следующий. Ученые знают, что в 6,25 граммах белка содержится один грамм азота. Чтобы определить белковый объем, достаточно умножить текущее количество азота на 6,25.


Тонкости строения
При рассмотрении вопроса, из чего состоят белки, стоит изучить и структуру этого вещества. Выделяют:
- Первичную структуру. За основу берется чередование аминокислот в составе. Если включается или «выпадает» хотя бы один элемент, то формируется новая молекула. Благодаря такой особенности, общее число последних достигает астрономической цифры.
- Вторичную структуру. Особенность молекул в составе белка такова, что они находятся не в растянутом состоянии, а имеют различные (иногда сложные) конфигурации. Благодаря этому, жизнедеятельность клетки упрощается. Вторичная структура имеет вид спирали, сформированной из равномерных витков. При этом соседние витки отличаются тесной водородной связью. В случае многократного повторения устойчивость возрастает.
- Третичная структура формируется, благодаря способности упомянутой спирали укладываться в клубок. Стоит знать, что состав и строение белков во многом зависит от первичной структуры. Третичная база, в свою очередь, гарантирует удержание качественных связей между аминокислотами с различными зарядами.
- Четвертичная структура характерна для некоторых белков (гемоглобина). Последний формирует не одну, а несколько цепей, которые отличаются по первичной структуре.
Секрет молекул белка – в общей закономерности. Чем больше структурный уровень, тем хуже удерживаются между собой образующиеся химические связи. Так, вторичная, третичная и четвертичная структуры подвержены действию радиации, высоких температур и прочих условий окружающей среды. Итогом часто становится нарушение строения (денатурация). При этом простой белок в случае изменения структуры способен к быстрому восстановлению. Если же вещество подверглось негативному температурному действию или влиянию других факторов, то процесс денатурации необратим, а само вещество не подлежит восстановлению.
Свойства
Выше рассмотрено, что такое белки, определение этих элементов, структура и прочие важные вопросы. Но информация будет неполной, если не выделить главные свойства вещества (физические и химические).
Молекулярная масса белка – от 10 тысяч до одного миллиона (здесь многое зависит от типа). Кроме того, они растворимы в воде.
Отдельно стоит выделить общие черты белка с каллоидными растворами:
- Способность к набуханию. Чем больше вязкость состава, тем выше молекулярная масса.
- Медленная диффузия.
- Способность к диализу, то есть делению аминокислотных групп на другие элементы при помощи мембран полупроницаемого типа. Главное отличие рассматриваемых веществ – их неспособность проходить через мембраны.
- Двухфакторная устойчивость. Это значит, что белок по структуре гидрофилен. Заряд вещества напрямую зависит, из чего состоит белок, числа аминокислот и их свойств.
- Размер каждой из частиц составляет 1-100 нм.
Также белки имеют определенные сходства с истинными растворами. Главное – в способности образования гомогенных систем. При этом процесс формирования самопроизвольный и не нуждается в дополнительном стабилизаторе. Кроме того, белковые растворы обладают термодинамической устойчивостью.
Ученые выделяют особые аморфные свойства рассматриваемых веществ. Объясняется это наличием аминогруппы. Если белок представлен в виде водного раствора, то в нем существуют в равной степени различные смеси – катионная, биполяного иона, а также анионная форма.


Также к свойствам белка стоит отнести:
- Способность играть роль буфера, то есть реагировать аналогично слабой кислоте или основанию. Так, в организме человека присутствует два типа буферных систем – белковая и гемоглобиновая, участвующие в нормализации уровня гомеостаза.
- Перемещение в электрическом поле. В зависимости от количества аминокислот в белке, их массы и заряда меняется и скорость движения молекул. Такая функция применяется для разделения с помощью электрофореза.
- Высаливание (обратное осаждение). Если добавить к белковому раствору ионы аммония, щелочноземельные металлы и щелочные соли, эти молекулы и ионы конкурируют между собой за воду. На этом фоне гидратная оболочка удаляется, а белки перестают быть устойчивыми. В итоге они выпадают в осадок. Если же добавить определенный объем воды, то возможно восстановление гидратной оболочки.
- Чувствительность к внешнему воздействию. Стоит отметить, что в случае негативного внешнего влияния белки разрушаются, что приводит к потере многих химических и физических свойств. Кроме того, денатурация становится причиной разрыва главных связей, стабилизирующих все уровни структуры белка (кроме первичного).
Причин денатурации множество – негативное влияние органических кислот, действие щелочей или ионов тяжелых металлов, негативное влияние мочевины и различных восстановителей, приводящих к разрушению мостиков дисульфидного типа.
- Наличие цветных реакций с разными химическими элементами (зависит от аминокислотного состава). Такое свойство применяется в лабораторных условиях, когда требуется определить общее количество белка.
Итоги
Белок – ключевой элемента клетки, обеспечивающий нормальное развитие и рост живого организма. Но, несмотря на изученность вещества учеными, впереди предстоит еще много открытий, позволяющих глубже узнать тайну человеческого организма и его строения. Пока же каждый из нас должен знать, где образуются белки, в чем их особенности и для каких целей они необходимы.
2 сентября 2016
proteinfo.ru
что нам о нем известно?
Как известно, белки являются необходимой и основной составной частью любого живого организма. Именно они отвечают за обмен веществ и превращения энергии, которые неразрывно связаны практически со всеми процессами жизнедеятельности. Сухое вещество подавляющего большинства тканей и органов животных и человека, а также более 50% всех микроорганизмов, в основном состоят из белков (от 40% до 50%). При этом в растительном мире их удельный вес по сравнению со средней величиной меньше, а в животном – больше. Вместе с тем химический состав белков для многих людей все еще является неизвестным. Давайте еще раз вспомним, что же находится внутри этих высокомолекулярных природных полимеров.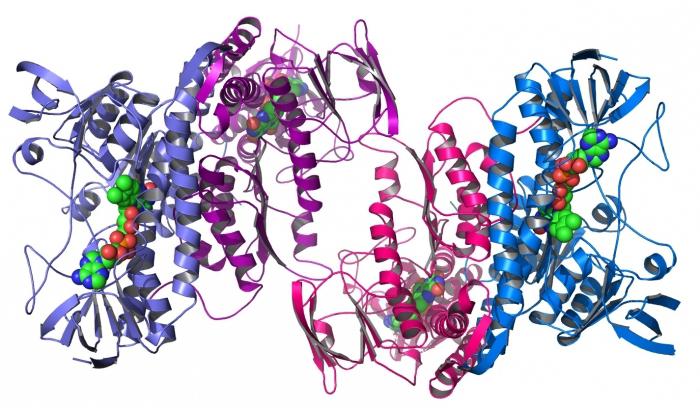
Состав белка
Это вещество в среднем содержат в себе примерно 50-55% углерода, 15-17% азота, 21-23% кислорода, 0,3-2,5% серы. Кроме перечисленных основных компонентов, порой в состав белков входят элементы, удельный вес которых очень незначителен. Прежде всего это фосфор, железо, йод, медь и некоторые другие микро- и макроэлементы. Любопытно, что концентрация азота обладает наибольшим постоянством, в то время как содержание других ключевых компонентов может варьироваться. Описывая состав белка, обязательно следует отметить, что он представляет собой нерегулярный полимер, построенный из остатков аминокислот, формулу которых в растворе воды при нейтральном pH в самом общем виде можно записать как Nh4+CHRCOO-.
Между собой эти «кирпичики» соединяются амидной связью между карбоксильными и аминными группами. Всего в природе выявлено около тысячи различных белков. К данному классу относятся антитела, ферменты, многие гормоны и прочие активные биологические вещества. Удивительно, но при всем таком разнообразии состав белка может включать не более 30 различных аминокислот, 20 из которых являются наиболее популярными. В человеческом организме их содержатся только 22, остальные же попросту не усваиваются и выводятся наружу. Восемь аминокислот из данной группы принято считать незаменимыми. Это лейцин, метионин, изолейцин, лизин, фенилаланин, триптофан, треонин и валин. Их наш организм самостоятельно синтезировать не может, а потому требуется их поступление извне.  Остальные же (таурин, аргинин, глицин, карнитин, аспарагин, гистидин, цистеин, глютамин, аланин, орнитин, тирозин, пролин, серин, цистин) он вполне может создать самостоятельно. Поэтому такие аминокислоты относят к группе заменимых. В зависимости от наличия в составе белка первой группы, а также от степени его усвоения организмом, белок делится на полноценный и неполноценный. Среднесуточная норма потребления данного вещества для человека лежит в диапазоне от 1 до 2 грамм на килограмм веса. При этом малоподвижным людям следует придерживаться нижней границы данного диапазона, а спорстменам - верхней.
Остальные же (таурин, аргинин, глицин, карнитин, аспарагин, гистидин, цистеин, глютамин, аланин, орнитин, тирозин, пролин, серин, цистин) он вполне может создать самостоятельно. Поэтому такие аминокислоты относят к группе заменимых. В зависимости от наличия в составе белка первой группы, а также от степени его усвоения организмом, белок делится на полноценный и неполноценный. Среднесуточная норма потребления данного вещества для человека лежит в диапазоне от 1 до 2 грамм на килограмм веса. При этом малоподвижным людям следует придерживаться нижней границы данного диапазона, а спорстменам - верхней.
Как изучают состав белка
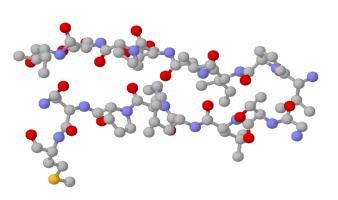
Для исследования данных веществ в основном применяется метод гидролиза. Вызывающий интерес белок нагревают с разбавленной соляной кислотой (6-10 моль/литр) при температуре от 100 ˚С до 1100 ˚С. В результате он распадется на смесь аминокислот, из которых уже выделяют отдельные аминокислоты. В настоящее время для количественного анализа исследуемого белка используют бумажную, а также ионообменную хроматографию. Существует даже особые автоматические анализаторы, которые легко определяют, какие именно аминокислоты образуются в результате распада.
fb.ru
2. 3. Химический состав белков.
Белки являются сложными органическими соединениями, состоящими из аминокислот. Химический анализ показал, что белки состоят из следующих элементов:
Углерод 50-55 %
Водород 6-7 %
Кислород 21-23 %
Азот 15-17 %
Сера 0,3-2,5 %.
В составе отдельных белков обнаружены также фосфор, йод, железо, медь и др. макро- и микровещества.
Содержание основных химических элементов может различаться в отдельных белках, исключение составляет азот, среднее количество которого характеризуется наибольшим постоянством и составляет 16 %. В связи с этим существует способ определения количества белка по входящему в его состав азоту. Зная, что 6,25 грамм белка содержит 1 грамм азота, можно найти количество белка, умножив найденное количество азота на коэффициент 6,25.
2. 4. Аминокислоты.
Аминокислоты – карбоновые кислоты альфа-углеродный атом водорода которых замещен на аминогруппу. Белки состоят из аминокислот. В настоящее время известно более 200 различных аминокислот. В организме человека их около 60, а в состав белков входят только 20 аминокислот, которые называют природными или протеиногенными. 19 из них являются альфа-аминокислотами, это означает, что аминогруппа присоединена к альфа-углеродному атому карбоновой кислоты. Общая формула этих аминокислот выглядит следующим образом.
R
h3N CH COOH
Только аминокислота пролин не соответствует этой формуле, её относят к иминокислотам.
Химические названия аминокислот, для краткости сокращают, например, глутаминовая кислота ГЛУ, серин СЕР и т.д. для записи первичной структуры белков в последнее время стали пользоваться только однобуквенными символами.
Во всех аминокислотах есть общие группировки: -СН2, -NН2, -СООН, они придают общие химические свойства белкам, и радикалы, химическая природа которых разнообразна. Именно они определяют структурные и функциональные особенности аминокислот.
Классификации аминокислот основана на их физико-химических свойствах.
По строению радикалов:
Циклические - гомоциклические ФЕН, ТИР, гетероциклические ТРИ, ГИС.
Ациклические – моноаминомонокарбоновые ГЛИ, АЛА, СЕР, ЦИС, ТРЕ, МЕТ, ВАЛ, ЛЕЙ, ИЛЕЙ,НЛЕЙ, моноаминодикарбоновые АСП, ГЛУ, диаминомонокарбоновые ЛИЗ, АРГ.
По образованию в организме:
Заменимые – могут синтезироваться в организме из веществ белковой и небелковой природы.
Незаменимые – не могут синтезироваться в организме, поэтому должны поступать только с пищей – все циклические аминокислоты, ТРЕ, ВАЛ, ЛЕЙ, ИЛЕЙ.
Биологическое значение аминокислот:
Входят в состав белков организма человека.
Входят в состав пептидов организма человека.
Из аминокислот образованы в организме многие низкомолекулярные биологически активные вещества: ГАМК, биогенные амины и т.д.
Часть гормонов в организме – производные аминокислот (гормоны щитовидной железы, адреналин).
Предшественники азотистых оснований, входящих в состав нуклеиновых кислот.
Предшественники порфиринов, идущих на биосинтез гема для гемоглобина и миоглобина.
Предшественники азотистых оснований, входящих в состав сложных липидов (холина, этаноламина).
Участвуют в биосинтезе медиаторов в нервной системе (ацетилхолин, дофамин, серотонин, норадреналин и др.).
Свойства аминокислот:
Хорошо растворимы в воде.
В водном растворе существуют в виде равновесной смеси биполярного иона, катионной и анионной форм молекулы. Равновесие зависит от рН среды.
Nh4—CH—COOH Nh4—CH—COO Nh3—CH—COO
R + ОН R R + Н
Катионная форма Биполярный ион Анионная форма
Щелочная среда рН Кислая среда
Способны двигаться в электрическом поле, что используется для разделения аминокислот с помощью электрофореза.
Проявляют амфотерные свойства.
Могут играть роль буферной системы, т.к. могут реагировать как слабое основание и слабая кислота.
studfiles.net
Состав и строение белков
В основе жизнедеятельности клетки лежат биохимические процессы, протекающие на молекулярном уровне и служащие предметом изучения биохимии. Соответственно и явления наследственности и изменчивости тоже связаны с молекулами органических веществ, и в первую очередь с нуклеиновыми кислотами и белками.
Состав белков
Белки представляют собой большие молекулы, состоящие из сотен и тысяч элементарных звеньев - аминокислот. Такие вещества, состоящие из повторяющихся элементарных звеньев — мономеров, называются полимерами. Соответственно белки можно назвать полимерами, мономерами которых служат аминокислоты.
Всего в живой клетке известно 20 видов аминокислот. Название аминокислоты получили из-за содержания в своем составе аминной группы NHy, обладающей основными свойствами, и карбоксильной группы СООН, имеющей кислотные свойства. Все аминокислоты имеют одинаковую группу Nh3—СН—СООН и отличаются друг от друга химической группой, называемой радикалом - R. Соединение аминокислот в полимерную цепь происходит благодаря образованию пептидной связи (СО - NH) между карбоксильной группой одной аминокислоты и аминогруппой другой аминокислоты. При этом выделяется молекула воды. Если образовавшаяся полимерная цепь короткая, она называется олигопептидной, если длинная - полипептидной.
Строение белков
При рассмотрении строения белков выделяют первичную, вторичную, третичную структуры.
Первичная структура определяется порядком чередования аминокислот в цепи. Изменение в расположении даже одной аминокислоты ведет к образованию совершенно новой молекулы белка. Число белковых молекул, которое образуется при сочетании 20 разных аминокислот, достигает астрономической цифры.
Если бы большие молекулы (макромолекулы) белка располагались в клетке в вытянутом состоянии, они занимали бы в ней слишком много места, что затруднило бы жизнедеятельность клетки. В связи с этим молекулы белка скручиваются, изгибаются, свертываются в самые различные конфигурации. Так на основе первичной структуры возникает вторичная структура — белковая цепь укладывается в спираль, состоящую из равномерных витков. Соседние витки соединены между собой слабыми водородными связями, которые при многократном повторении придают устойчивость молекулам белков с этой структурой.
Спираль вторичной структуры укладывается в клубок, образуя третичную структуру. Форма клубка у каждого вида белков строго специфична и полностью зависит от первичной структуры, т. е. от порядка расположения аминокислот в цепи. Третичная структура удерживается благодаря множеству слабых электростатических связей: положительно и отрицательно заряженные группы аминокислот притягиваются и сближают даже далеко отстоящие друг от друга участки белковой цепи. Сближаются и иные участки белковой молекулы, несущие, например, гидрофобные (водоотталкивающие) группы.
Некоторые белки, например гемоглобин, состоят из нескольких цепей, различающихся по первичной структуре. Объединяясь вместе, они создают сложный белок, обладающий не только третичной, но и четвертичной структурой (рис. 2).
В структурах белковых молекул наблюдается следующая закономерность: чем выше структурный уровень, тем слабее поддерживающие их химические связи. Связи, образующие четвертичную, третичную, вторичную структуру, крайне чувствительны к физико-химическим условиям среды, температуре, радиации и т. д. Под их воздействием структуры молекул белков разрушаются до первичной — исходной структуры. Такое нарушение природной структуры белковых молекул называется денатурацией. При удалении денатурирующего агента многие белки способны самопроизвольно восстанавливать исходную структуру. Если же природный белок подвергается действию вьюокой температуры или интенсивному действию других факторов, то он необратимо денатурируется. Именно фактом наличия необратимой денатурации белков клеток объясняется невозможность жизни в условиях очень высокой температуры.
Первичная структура белков.

Вторичная структура белков.
Третичная структура белков.
Четвертичная структура белков.
Биологическая роль белков в клетке
Белки, называемые также протеинами (греч. протос — первый}, в клетках животных и растений выполняют многообразные и очень важные функции, к которым можно отнести следующие.
Каталитическая. Природные катализаторы — ферменты представляют собой полностью или почти полностью белки. Благодаря ферментам химические процессы в живых тканях ускоряются в сотни тысяч или в миллионы раз. Под их действием все процессы идут мгновенно в «мягких» условиях: при нормальной температуре тела, в нейтральной для живой ткани среде. Быстродействие, точность и избирательность ферментов несопоставимы ни с одним из искусственных катализаторов. Например, одна молекула фермента за одну минуту осуществляет реакцию распада 5 млн. молекул пероксида водорода (Н202). Ферментам характерна избирательность. Так, жиры расщепляются специальным ферментом, который не действует на белки и полисахариды (крахмал, гликоген). В свою очередь, фермент, расщепляющий только крахмал или гликоген, не действует на жиры.
Процесс расщепления или синтеза любого вещества в клетке, как правило, разделен на ряд химических операций. Каждую операцию выполняет отдельный фермент. Группа таких ферментов составляет биохимический конвейер.
Считают, что каталитическая функция белков зависит от их третичной структуры, при ее разрушении каталитическая активность фермента исчезает.
Защитная. Некоторые виды белков защищают клетку и в целом организм от попадания в них болезнетворных микроорганизмов и чужеродных тел. Такие белки носят название антител. Антитела связываются с чужеродными для организма белками бактерий и вирусов, что подавляет их размножение. На каждый чужеродный белок организм вырабатывает специальные «антибелки» — антитела. Такой механизм сопротивления возбудителям заболеваний называется иммунитетом.
Чтобы предупредить заболевание, людям и животным вводят ослабленные или убитые возбудители (вакцины), которые не вызывают болезнь, но заставляют специальные клетки организма производить антитела против этих возбудителей. Если через некоторое время болезнетворные вирусы и бактерии попадают в такой организм, они встречают прочный защитный барьер из антител.
Гормональная. Многие гормоны также представляют собой белки. Наряду с нервной системой гормоны управляют работой разных органов (и всего организма) через систему химических реакций.
Отражательная. Белки клетки осуществляют прием сигналов, идущих извне. При этом различные факторы среды (температурный, химический, механический и др.) вызывают изменения в структуре белков — обратимую денатурацию, которая, в свою очередь, способствует возникновению химических реакций, обеспечивающих ответ клетки на внешнее раздражение. Эта способность белков лежит в основе работы нервной системы, мозга.
Двигательная. Все виды движений клетки и организма: мерцание ресничек у простейших, сокращение мышц у высших животных и другие двигательные процессы — производятся особым видом белков.
Энергетическая. Белки могут служить источником энергии для клетки. При недостатке углеводов или жиров окисляются молекулы аминокислот. Освободившаяся при этом энергия используется на поддержание процессов жизнедеятельности организма.
Транспортная. Белок гемоглобин крови способен связывать кислород воздуха и транспортировать его по всему телу. Эта важнейшая функция свойственна и некоторым другим белкам.
Пластическая. Белки — основной строительный материал клеток (их мембран) и организмов (их кровеносных сосудов, нервов, пищеварительного тракта и др.). При этом белки обладают индивидуальной специфичностью, т. е. в организмах отдельных людей содержатся некоторые, характерные лишь для него, белки-
Таким образом, белки — эти важнейший компонент клетки, без которого невозможно проявление свойств жизни. Однако воспроизведение живого, явление наследственности, как мы увидим позже, связано с молекулярными структурами нуклеиновых кислот. Это открытие — результат новейших достижений биологии. Теперь известно, что живая клетка обязательно обладает двумя видами полимеров—белками и нуклеиновыми кислотами. В их взаимодействии заключены самые глубокие стороны явления жизни.
biofile.ru
|
Строительная: Белки участвуют в образовании клеточных и внеклеточных структур: входят в состав клеточных мембран (липопротеины, гликопротеины), волос (кератин), сухожилий (коллаген) и т.д. |
|
|
Транспортная: |
Белок крови гемоглобин присоединяет кислород и транспортирует его от легких ко всем тканям и органам, а от них в легкие переносит углекислый газ; в состав клеточных мембран входят особые белки, которые обеспечивают активный и строго избирательный перенос некоторых веществ и ионов из клетки во внешнюю среду и обратно. |
|
Регуляторная: Гормоны белковой природы принимают участие в регуляции процессов обмена веществ. Например, гормон инсулин регулирует уровень глюкозы в крови, способствует синтезу гликогена, увеличивает образование жиров из углеводов. |
|
|
Защитная: В ответ на проникновение в организм чужеродных белков или микроорганизмов (антигенов) образуются особые белки - антитела, способные связывать и обезвреживать их. Фибрин, образующийся из фибриногена, способствует остановке кровотечений. |
|
|
Двигательная: Сократительные белки актин и миозин обеспечивают сокращение мышц у многоклеточных животных. |
|
|
Сигнальная: В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды, таким образом осуществляя прием сигналов из внешней среды и передачу команд в клетку. |
|
|
Запасающая: В организме животных белки, как правило, не запасаются, исключение: альбумин яиц, казеин молока. Но благодаря белкам в организме могут откладываться про запас некоторые вещества, например, при распаде гемоглобина железо не выводится из организма, а сохраняется, образуя комплекс с белком ферритином. |
|
|
Энергетическая: При распаде 1 г белка до конечных продуктов выделяется 17,6 кДж. Сначала белки распадаются до аминокислот, а затем до конечных продуктов - воды, углекислого газа и аммиака. Однако в качестве источника энергии белки используются только тогда, когда другие источники (углеводы и жиры) израсходованы. |
|
|
Каталитическая: Одна из важнейших функций белков. Обеспечивается белками - ферментами, которые ускоряют биохимические реакции, происходящие в клетках. Например, рибулезобифосфаткарбоксилаза катализирует фиксацию СО2 при фотосинтезе. Copyright © BioFile 2007-2016 |
biofile.ru
Строение белков
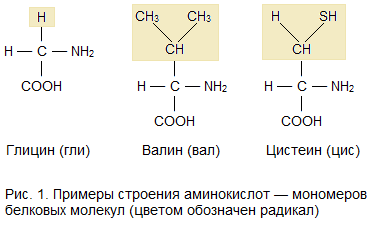
Среди органических веществ белки, или протеины, — самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 — 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами. Кроме углерода, кислорода, водорода и азота, в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
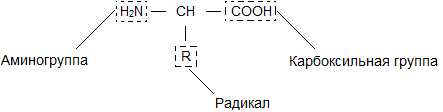
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (—Nh3) с основными свойствами, другая — карбоксильной группой (—COOH) с кислотными свойствами. Часть молекулы, называемая радикалом (R), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами.
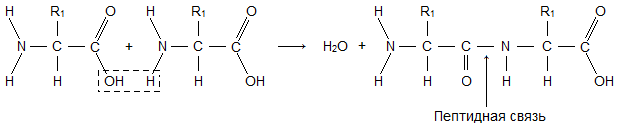
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру белка. Она уникальна для любого белка и определяет его форму, свойства и функции.Большинство белков имеют вид спирали в результате образования водородных связей между —CO- и —NH- группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль — вторичная структура белка.
Третичная структура — трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация — глобула. Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.Нарушение природной структуры белка называют денатурацией. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остается в виде полипептидной цепи.Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков, состоящих только из аминокислот, есть еще и сложные белки
Другие заметки по биологии
edu.glavsprav.ru
Белки в химическом составе организма
Белки выполняют в организме очень важные функции. К ним в первую очередь следует отнести: структурную, каталитическую, сократительную, транспортную, регуляторную, защитную, а также энергетическую. На долю белков в среднем приходится 1/6 часть от массы тела человека.
По строению белки - это высокомолекулярные азотсодержащие соединения, состоящие из аминокислот. В состав белковых молекул могут входить десятки, сотни и тысячи остатков аминокислот. Однако все белки, независимо от происхождения, содержат лишь 20 видов аминокислот Строение 20 разновидностей аминокислот, входящих во все белки, можно отразить следующей формулой:

У всех аминокислот можно выделить общую, одинаковую часть молекулы, содержащую амино- и карбоксильную группы (выделена пунктирной рамкой). Другая же часть молекулы, обозначенная как радикал (R), у каждой из 20 аминокислот имеет специфическое строение, и аминокислоты отличаются друг от друга только радикалами.
Аминокислоты, соединяясь друг с другом пептидной связью, образуют длинные неразветвленные цепи - полипептиды. Пептидная связь возникает при взаимодействии карбоксильной группы одной аминокислоты и аминогруппы другой аминокислоты с выделением воды:

Пептидные связи обладают высокой прочностью, их образуют все аминокислоты.
В состав белковой молекулы входит один или несколько полипептидов.
Кроме пептидных, в белках обнаруживаются еще дисульфидные, водородные, ионные и другие связи.
Эти химические связи могут возникать между остатками аминокислот, которые входят в разные участки одного и того же полипептида или же находятся в разных полипептидах, но обязательно пространственно сближены. В первом случае благодаря таким связям полипептидная цепь принимает определенную пространственную форму. Во втором случае с помощью непептидных связей полипептиды объединяются в белковую молекулу.
В итоге молекула белка является объемным, трехмерным образованием, имеющим определенную пространственную форму. Для удобства рассмотрения пространственного строения молекулы белка условно выделяют четыре уровня ее структурной организации.
Первый уровень пространственной организации белковой молекулы называется первичной структурой и представляет собой последовательность расположения аминокислот в полипептидных цепях. Фиксируется эта структура прочными пептидными связями. Другими словами, первичная структура характеризует химическое строение полипептидов, образующих белковую молекулу. Каждый индивидуальный белок имеет уникальную первичную структуру.
Второй уровень пространственной организации - вторичная структура - описывает пространственную форму полипептидных цепей. Например, у многих белков полипептидные цепи имеют форму спирали. Фиксируется вторичная структура дисульфидными и различными нековалентными связями.
Третий уровень пространственной организации - третичная структура - отражает пространственную форму вторичной структуры. Например, вторичная структура в форме спирали, в свою очередь, может укладываться в пространстве в виде глобулы, т. е. имеет шаровидную или яйцевидную форму. Стабилизируется третичная структура слабыми нековалентными связами, а также дисульфидными связями и поэтому является самой неустойчивой структурой.
Пространственная форма всей белковой молекулы получила название конформация. Поскольку в молекуле белка наряду с прочными ковалентными связями имеются еще менее прочные (нековалентные) связи, то его конформация характеризуется нестабильностью и может легко изменяться. Изменение пространственной формы белка влияет на его биологические функции. Конформация, находясь в которой белок обладает биологической активностью, называется нативной. Любые воздействия на белок, приводящие к нарушению этой конформации, сопровождаются частичной или полной утратой белком его биологических свойств. Изменение конформации в небольших пределах обратимо и является одним из механизмов регуляции биологических функций белков в организме.
Четвертичной структурой обладают только некоторые белки. Четвертичная структура - это сложное надмолекулярное образование, состоящее из нескольких белков, имеющих свою собственную первичную, вторичную и третичную структуры. Каждый белок, входящий в состав четвертичной структуры, называется субъединицей. Например, белок крови гемоглобин состоит из четырех субъединиц двух типов (а и Р) и имеет строение а2рг- Ассоциация субъединиц в четвертичную структуру приводит к возникновению нового биологического свойства, отсутствующего у свободных субъединиц. Например, формирование четвертичной структуры в ряде случаев сопровождается появлением каталитической активности, которой нет у отдельных субъединиц.
Объединяются субъединицы в четвертичную структуру за счет слабых нековалентных связей, и поэтому четверичная структура неустойчива и легко диссоциирует на субъединицы. Образование и диссоциация четвертичной структуры является еще одним механизмом регуляции биологических функций белков.
Из всех структур белка кодируется только первичная. За счет информации, заключенной в молекуле ДНК, синтезируются полипептидные цепи (первичная структура). Высшие структуры (вторичная, третичная, четвертичная) возникают самопроизвольно в соответствии со строением полипептидов.
Классификация белков
Белки делятся на простые (протеины) и сложные (протеиды). Простые белки состоят только из аминокислот. К простым белкам, имеющимся в организме человека, относятся альбумины, глобулины, гистоны, белки опорных тканей. В молекуле сложного белка, кроме аминокислот, еще имеется неаминокислотная часть, называемая простетической группой. В зависимости от строения простетической группы выделяют такие сложные белки, как фосфопротеиды (содержат в качестве простетической группы фосфорную кислоту), нуклеопротеиды (содержат нуклеиновую кислоту), гликопротеиды (содержат углевод), липопротеиды (содержат липоид), хромопротеиды (содержат окрашенную простетическую группу) и др.
Возможна и другая классификация белков, вытекающая из их пространственной формы. В этом случае белки разделяются на два больших класса: глобулярные и фибриллярные.
Молекулы глобулярных белков имеют шарообразную или эллипсоидную форму. Примером таких белков являются альбумины и глобу лины плазмы крови.
Фибриллярные белки представляют собою вытянутые молекулы, у которых длина значительно превышает их диаметр. К таким белкам прежде всего необходимо отнести коллаген - самый распространенный белок у человека и высших животных, на долю которого приходится 25-30% от общего количества белков организма. Коллаген обладает высокой прочностью и эластичностью. Этот белок широко распространен в организме, он входит в состав соединительной ткани, и поэтому его можно обнаружить в коже, стенках сосудов, мышцах, сухожилиях, хрящах, костях, во внутренних органах.
biofile.ru





.jpg)





