Урок природоведения по теме: "Ее величество — вода". 5-й класс. При нагревании вода
Почему вода бывает легче самой воды?!
Одно из самых распространенных веществ на Земле: вода. Она, как и воздух, необходима нам, но мы ее порой совсем не замечаем. Она просто есть. Но, оказывается
Одно из самых распространенных веществ на Земле: вода. Она, как и воздух, необходима нам, но мы ее порой совсем не замечаем. Она просто есть. Но, оказывается, обыкновенная вода может менять свой объем и весить то больше, то меньше. При испарении воды, ее нагревании и охлаждении происходят поистине удивительные вещи, о которых мы и узнаем сегодня.Мюриэль Мэнделл в своей занимательной книге «Phycisc Experiments for Children» излагает интереснейшие мысли о свойствах воды, на основе которых не только юные физики могут узнать немало нового, но и взрослые освежат свои знания, которые давненько не приходилось применять, поэтому они оказались слегка забытыми.Сегодня речь пойдет об объеме и весе воды. Оказывается, один и тот же объем воды не всегда весит одинаково. И если налить воду в стакан и она не прольется через край — это еще не значит, что она поместится в нем при любых обстоятельствах.
1. При нагревании вода увеличивается в объеме
Поставьте наполненную водой банку в кастрюлю, наполненную сантиметров на пять кипящей водой, и на слабом огне поддерживайте кипение. Вода из банки начнет переливаться через край. Это происходит потому, что при нагревании вода, подобно другим жидкостям, начинает занимать больше пространства. Молекулы отталкиваются друг от друга с большей интенсивностью и это ведет к увеличению объема воды.2. При охлаждении вода сжимается
Дайте воде в банке остыть при комнатной температуре, или налейте новую воду, и поставьте ее в холодильник. Через некоторое время вы обнаружите, что полная прежде банка уже не полна. При охлаждении до температуры 3,89 градусов по Цельсию вода уменьшает свой объем по мере снижения температуры. Причиной тому стало снижение скорости движения молекул и их сближение друг с другом под воздействием охлаждения. Казалось бы, все очень просто: чем холоднее вода, тем меньший объем она занимает, но…
3. …объем воды вновь возрастает при замерзании
Наполните банку водой до краев и накройте куском картона. Поставьте ее в морозилку и дождитесь замерзания. Вы обнаружите, что картонную «крышку» вытолкнуло. На температурном интервале между 3,89 и 0 градусов по Цельсию, то есть на подходе к точке своего замерзания, вода вновь начинает расширяться. Она является одним из немногих известных веществ, обладающих подобным свойством. Если использовать плотную крышку, то лед просто разнесет банку. Приходилось ли вам слышать о том, что даже водопроводные трубы может разорвать льдом?4. Лед легче воды
Поместите пару кубиков льда в стакан с водой. Лед будет плавать на поверхности. Вода при замерзании увеличивается в объеме. И, вследствие этого, лед легче воды: его объем составляет около 91% соответствующего объема воды. Это свойство воды существует в природе не зря. У него есть вполне определенное предназначение. Говорят, что зимой реки замерзают. Но на самом деле это не совсем верно. Обычно замерзает лишь небольшой верхний слой. Это ледяной покров не тонет, поскольку он легче жидкой воды. Он замедляет замерзание воды на глубине реки и служит своеобразным одеялом, оберегая рыб и другую речную да озерную живность от лютых зимних морозов. Изучая физику, начинаешь понимать, что очень многое в природе устроено целесообразно.5. Водопроводная вода содержит минералы
Влейте в небольшую стеклянную миску 5 столовых ложек обычной водопроводной воды. Когда вода испарится, на миске останется белая кайма. Эта кайма сформирована минералами, которые были растворены в воде, когда она проходила слои грунта. Посмотрите внутрь своего чайника и вы увидите там минеральный налет. Такой же налет образуется и на отверстии для стока воды в ванне. Попробуйте испарить дождевую воду, чтобы самостоятельно проверить, содержит ли она минералы.econet.ru
Содержание
У самого распространенного на планете Земля вещества – воды – есть одна особенность, которая отличает его от прочих жидкостей. При нагревании вода имеет свойство расширяться, однако лишь с 4оС. А вот в пределах от 0 до 4оС происходит противоположный процесс – вода уменьшается. Благодаря этому свойству при замерзании поверхности воды в глубинах водоемов продолжают жить рыбы и иные обитатели водного мира. Удивительные свойства водыВоде присущи поразительные свойства, которые сильно отличают ее от прочих жидкостей. Но это и хорошо, иначе, обладай вода «обычными» свойствами, планета Земля была бы абсолютно другой. Для подавляющего большинства веществ характерно при нагревании расширяться. Что довольно легко объяснить с позиции механической теории теплоты. Согласно ей, при нагревании атомы и молекулы вещества начинают двигаться быстрее. В твердых телах колебания атомов достигают большей амплитуды, и им необходимо больше свободного пространства. Как результат – происходит расширение тела. Тот же самый процесс происходит и с жидкостями, и с газами. То есть, за счет повышения температуры увеличивается скорость теплового движения свободных молекул, и тело расширяется. При охлаждении же, соответственно, происходит сжатие тела. Это свойственно практически для всех веществ. За исключением воды. При охлаждении в интервале от 0 до 4оС вода расширяется. И сжимается – при нагревании. Когда отметка температуры воды достигает 4оС, в этот момент вода имеет максимальную плотность, которая равна 1000 кг/м3. Если температура ниже или выше этой отметки, то плотность всегда немного меньше. Благодаря этому свойству при понижении температуры воздуха осенью и зимой в глубоких водоемах происходит интересный процесс. Когда вода охлаждается, она опускается ниже, на дно, однако лишь до того момента, пока ее температура не станет +4оС. Именно по этой причине в больших водоемах более холодная вода находится ближе к поверхности, а более теплая – опускается на дно. Так что когда зимой поверхность воды замерзает, более глубокие слои продолжают сохранять температуру 4оС. Благодаря этому моменту рыба может спокойно зимовать в глубинах покрывшихся льдом водоемов.Влияние расширения воды на климатИсключительные свойства воды при нагревании серьезным образом влияют на климат Земли, поскольку около 79% поверхности нашей планеты покрыто водой. За счет солнечных лучей происходит нагревание верхних слоев, которые затем опускаются ниже, а на их месте оказываются холодные слои. Те тоже, в свою очередь, постепенно нагреваются и опускаются ближе ко дну. Таким образом, слои воды непрерывно меняются, что приводит к равномерному прогреванию, пока не достигается температура, соответствующая максимальной плотности. Затем, нагреваясь, верхние слои становятся менее плотными и уже не опускаются вниз, а остаются наверху и просто постепенно становятся теплее. За счет этого процесса огромные толщи воды довольно легко прогреваются солнечными лучами. |
completerepair.ru
"Ее величество — вода". 5-й класс

Разделы: Биология
Цели урока:
- расширить знания о воде, ее свойствах, значении воды, ввести понятия раствор, взвесь, значение растворов в природе и жизни человека;
- развить наблюдательность, мыслительную деятельность, воспитывать бережное отношение к воде.
Оборудование:
- химическая посуда для опытов,
- спиртовка,
- вещества для опытов,
- костюмы для капелек, к
- арточки для самостоятельной работы.
Ход урока
Здравствуйте, ребята! Сегодня наш урок посвящен воде и называется “Ее величество – вода”. На уроке мы расширим свои знания о воде, познакомимся с ее свойствами, а также водой как растворителем веществ. Узнаем, что такое раствор и, что такое взвесь.
Открываем тетради, в которых записываем тему урока “Ее величество – вода”.
Каждый человек пользуется водой для приготовления пищи и других бытовых нужд, для промышленных предприятий, для выращивания растений и животных. Что же такое вода расскажут нам капельки.
Капелька 1: Вода – вещество привычное и необычное. Ученые абсолютно правы: нет на Земле вещества более важного для нас, чем обыкновенная вода. Почти три четверти поверхности нашей планеты занято морями и океанами. Твердой водой - снегом и льдом - покрыто 20% суши. От воды зависит климат нашей планеты. Земля давно бы остыла и превратилась в безжизненный камень, если бы не вода. Нагреваясь вода забирает тепло, а остывая отлает его. От космического холода предохраняет Землю та вода, которая рассеяна в атмосфере – в облаках в виде пара.
Капелька 2: У воды много удивительных свойств, которые делают ее не похожей на все другие вещества. Но среди них есть одно необычное - это ее бессмертие. Примерно один миллиард тонн воды расходуется человечеством за сутки. Но общее количество воды не уменьшается. Сколько ее было миллионы лет назад, столько же ее и в наше время.
Капелька 3: Велика роль воды в жизни на Земле. Живые организмы нашей планеты приспособились ко всяким условиям: к полному мраку, к жаре и холоду. Но ни одно живое существо не может обходиться без воды. Все растения и животные содержат в себе воду, да и наше собственное тело на три четверти состоит из воды. Знаете ли вы, что при потере человеком 1 литра воды (это примерно 2% массы тела) появляется ощущение жажды. При потери 6-8% влаги человек впадает в полуобморочное состояние. Потеря 10% воды вызывает галлюцинации. А потеря более 12% человек погибает.
Учитель: Так что же такое вода? (Ответы детей) Вода – это химическое вещество, которое имеет свои свойства. В тетрадях записываем: Свойства воды.
С некоторыми свойствами воды вы уже знакомы. Давайте вспомним их, а поможет нам в этом наш учебник (работа с учебником).
Свойства воды:
- прозрачна;
- бесцветна;
- без вкуса и без запаха;
- текуча;
- может находиться в трех агрегатных состояниях;
- может переходить из одного агрегатного состояния в другое.
(Свойства воды записываются в тетрадь)
А теперь давайте познакомимся еще с некоторыми ее свойствами. В этом помогут нам опыты.
ОПЫТ 1:
Оборудование:
- 2 колбы с газоотводной трубкой,
- 2 кристаллизатора.
Вещества:
- вода,
- горячая вода,
- лед.
Посмотрим, что произойдет, если мы возьмем две одинаковые колбы с водой, уровень воды отметим меткой. Одну опустим в лед, а другую в горячую воду. Что происходит?
Мы наблюдаем, что в горячей воде, вода находящаяся в колбе поднимается выше метки, а в колбе, которую опускаем в лед, наоборот опускается.
Делаем вывод, что вода при нагревании расширяется, а при охлаждении сжимается.
Давайте посмотрим другой опыт.
ОПЫТ 2:
(Опыт демонстрируется учеником как выполненное домашнее задание)
Оборудование:
- стеклянная бутылка с пробкой.
Вещество:
Ученик: Я взял стеклянную бутылку, налил воды, плотно заткнул пробкой и вынес на мороз. Когда вода замерзла, бутылка лопнула и раскололась на куски. Это произошло потому, что при замерзании вода расширяется.
Однажды ученые поставили опыт, подобный этому, но вместо бутылки взяли чугунный шар, наполнили его водой, завинтили отверстия и поставили на сильный мороз. Вода, замерзая, разорвала шар. Так велика сила расширяющейся воды.
Учитель: Ребята, после демонстрации опытов какой можно сделать вывод? Какими свойствами наряду с теми которые мы записали обладает вода? (Ответы детей)
Давайте в своих тетрадях запишем свойства воды:
- вода при нагревании расширяется;
- вода при охлаждении сжимается;
- вода при замерзании расширяется.
Пришло время закрепить полученные на нашем уроке знания. Ответьте мне, пожалуйста, на вопросы:
- Если в чайник или кастрюлю налить воду до краёв и начать нагревать, то через некоторое время вода начинает выплескиваться через край. Почему это происходит? (Вода при нагревании расширяется)
- Почему садоводы перед наступлением зимы обязательно спускают воду с труб на садовом участке? (При замерзании вода расширяется и поэтому чтобы трубы не лопнули садоводы сливают воду)
- Вода попадает в мельчайшие трещины скал, от чего горные породы разрушаются. С каким свойством воды это связанно? (Разрушение горных пород связано с расширением воды при замерзании)
- Известно, что при длительном нагревании вода закипает. Температура кипения равна сто градусов. Кипящая вода используется в быту и на производстве. Где в природе можно встретить горячую воду? (В гейзерах).
Закрепив полученные знания мы следуем дальше, знакомясь с удивительным веществом природы – водой.
При нагревании и кипячении над водой поднимается пар – происходит испарение. Давайте в своих тетрадях запищим определение (работа с тетрадями).
Испарение – это превращение жидкой воды в газообразную.
Испарение происходит при любой температуре, но при более высокой испарение протекает более быстрее. Например: лужи после дождя высыхают и жарким летом и холодной осенью, но летом высыхают быстрее чем осенью.
ОПЫТ З:
(Опыт демонстрируется группой учеников как выполненное домашнее задание)
Оборудование: мерный стакан, 3 чашки, 4 одинаковых стакана.
Вещество:
Ученик: Мы взяли мерный стакан и отмерили в каждую чашку по 100 мл воды. Чашки с водой поставили одну на подоконник, другую на стол, третью возле батареи. На следующий день сравнили результаты. Взяли одинаковые стаканы в первый налили 100 мл воды (контроль), а в три остальные вылили воду из чашек. Сравниваем полученные результаты: вода из чашки стоявшей на подоконнике испарилась на одну треть, в чашке, которая стояла на столе - на половину, а чашка, стоящая у батареи была вообще сухая – вода испарилась полностью. Сделаем вывод: чем больше температура окружающей среды, тем испарение происходит быстрее.
Учитель: Со значением испарения в жизни человека и животных мы познакомимся на страницах учебника (работа с учебником).
Ответьте мне на вопросы для закрепления.
- Что такое испарение воды? (Превращение жидкой воды в газообразную)
- Как влияет температура и ветер на испарение воды? (Чем выше температура и сильнее ветер, тем испарение происходит быстрее)
- Когда быстрее высохнет бельё: в ветреную или безветренную погоду? (В ветреную)
Посмотрим еще один опыт.
ОПЫТ 4:
Оборудование:
- спиртовка,
- штативы,
- колба с газоотводной трубкой,
- металлическая пластина.
Вещество:
Колбу с водой нагреваем на спиртовке так, чтобы вода закипела, к газоотводной трубке подносим холодную пластину. Пар оседает на пластине в виде капелек.
Вывод: происходит превращение газообразной воды в жидкую.
Этот процесс называется конденсация.
(В тетрадях записываем)
Конденсация – это превращение водяного пара в воду.
Где мы встречаемся с этим явлением? Узнаем из рассказа.
Ученик: С конденсацией водяного пара мы встречаемся в повседневной жизни. Летним вечером или ранним утром, когда воздух холоднее, выпадает роса. Это водяной пар, находящийся в воздухе, при охлаждении оседает на траве, листьях и других предметах в виде маленьких капелек воды. Облака также образуется в результате конденсации водяного пара. Поднимаясь над землей и водоемами в верхние, более холодные слои воздуха, этот пар и образует облака, состоящие из маленьких капелек воды. Если температура воздуха достаточна низкая, то капельки воды замерзают. Из таких облаков выпадает снег, а иногда и град.
Учитель: Спасибо за сообщение.
А сейчас давайте проведем не большую лабораторную работу. На столах у вас находиться все необходимое для работы: химическая посуда и вещества: вода, мел, соль.
Возьмите соль и растворите в воде. Что наблюдаете? (Соль растворилась). Мы получили раствор соли.
Это можно записать схематично так:
растворитель + растворимое вещество = раствор
вода + соль = раствор соли
А теперь возьмем мел, растворим его в воде и сравним с раствором соли. Что мы наблюдаем? (Раствор мела мутный). Профильтруем полученный раствор. Что наблюдаем? (Фильтрат прозрачный, а на фильтре остался осадок). Исходная жидкость называется взвесь.
Вывод:
- если частицы вещества не видимы в воде и вместе с водой проходят через фильтр, то такое вещество называют растворимым, а состояние раствором.
- если вещество плавает в воде, задерживается на фильтре, то это вещество не растворимое, а состояние взвесью.
Вода настолько уникальный растворитель, что имеет самое почтительное уважение.
Сегодня мы познакомились со свойствами воды. Теперь вы знаете, что вода при нагревании расширяется, при охлаждении сжимается, при замерзании расширяется. Вы также знает, что такое испарение и конденсация и какое значение они имеют, что такое раствор и взвесь. А теперь проверим, как вы усвоили новый материал.
Самостоятельная работа по карточкам
(Дописать нужные слова вместо точек)
- Вода при нагревании …………………………………………………………..
- Вода при охлаждении …………………………………………………………
- Вода при замерзании ……………………………………………………….
- Вода кипит при температуре …………………………………………………
- Превращение жидкой воды в газообразную- это …………………………..
- Превращение пара в воду- это ……………………………………………….
- Что такое раствор? ………………………………………………………………
- Как отличить раствор от взвеси? ………………………………………………..
Работы сдаем.
На этом наш урок закончен. Всем спасибо. До свидания.
xn--i1abbnckbmcl9fb.xn--p1ai
Предложена новая теория, объясняющая, почему вода при нагревании от 0 до 4°C сжимается
Японский физик Масакадзу Мацумото выдвинул теорию, которая объясняет, почему вода при нагревании от 0 до 4°C сжимается, вместо того чтобы расширяться. Согласно его модели, вода содержит микрообразования — «витриты», представляющие собой выпуклые пустотелые многогранники, в вершинах которых находятся молекулы воды, а ребрами служат водородные связи. При повышении температуры конкурируют между собой два явления: удлинение водородных связей между молекулами воды и деформация витритов, приводящая к уменьшению их полостей. В диапазоне температур от 0 до 3,98°C последнее явление доминирует над эффектом удлинения водородных связей, что в итоге и дает наблюдаемое сжатие воды. Экспериментального подтверждения модели Мацумото пока что нет — впрочем, как и других теорий, объясняющих сжатие воды.
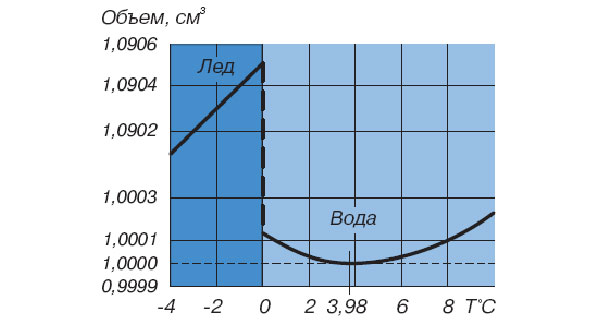
В отличие от подавляющего большинства веществ, вода при нагревании способна уменьшать свой объем (рис. 1), то есть обладает отрицательным коэффициентом теплового расширения. Впрочем, речь идет не обо всём температурном интервале, где вода существует в жидком состоянии, а лишь об узком участке — от 0°C примерно до 4°C. При больших температурах вода, как и другие вещества, расширяется.
Между прочим, вода — не единственное вещество, имеющее свойство сжиматься при увеличении температуры (или расширяться при охлаждении). Подобным поведением могут «похвастать» еще висмут, галлий, кремний и сурьма. Тем не менее, в силу своей более сложной внутренней структуры, а также распространенности и важности в разнообразных процессах, именно вода приковывает внимание ученых (см. Продолжается изучение структуры воды, «Элементы», 09.10.2006).
Некоторое время назад общепринятой теорией, отвечающей на вопрос, почему вода увеличивает свой объем при понижении температуры (рис. 1), была модель смеси двух компонент — «нормальной» и «льдоподобной». Впервые эта теория была предложена в XIX веке Гарольдом Витингом и позднее была развита и усовершенствована многими учеными. Сравнительно недавно в рамках обнаруженного полиморфизма воды теория Витинга была переосмыслена. Отныне считается, что в переохлажденной воде существует два типа льдообразных нанодоменов: области, похожие на аморфный лед высокой и низкой плотности. Нагревание переохлажденной воды приводит к плавлению этих наноструктур и к появлению двух видов воды: с большей и меньшей плотностью. Хитрая температурная конкуренция между двумя «сортами» образовавшейся воды и порождает немонотонную зависимость плотности от температуры. Однако пока эта теория не подтверждена экспериментально.
С приведенным объяснением нужно быть осторожным. Не случайно здесь говорится лишь о структурах, которые напоминают аморфный лед. Дело в том, что наноскопические области аморфного льда и его макроскопические аналоги обладают разными физическими параметрами.
Японский физик Масакадзу Мацумото решил найти объяснение обсуждаемого здесь эффекта «с нуля», отбросив теорию двухкомпонентной смеси. Используя компьютерное моделирование, он рассмотрел физические свойства воды в широком диапазоне температур — от 200 до 360 К при нулевом давлении, чтобы в молекулярном масштабе выяснить истинные причины расширения воды при ее охлаждении. Его статья в журнале Physical Review Letters так и называется: Why Does Water Expand When It Cools? («Почему вода при охлаждении расширяется?»).
Изначально автор статьи задался вопросом: что влияет на коэффициент теплового расширения воды? Мацумото считает, что для этого достаточно выяснить влияние всего трех факторов: 1) изменения длины водородных связей между молекулами воды, 2) топологического индекса — числа связей на одну молекулу воды и 3) отклонения величины угла между связями от равновесного значения (углового искажения).
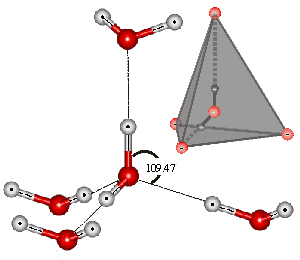
Перед тем как рассказать о результатах, полученных японским физиком, сделаем важные замечания и разъяснения по поводу вышеупомянутых трех факторов. Прежде всего, привычная химическая формула воды h3O соответствует лишь парообразному ее состоянию. В жидкой форме молекулы воды посредством водородной связи объединяются в группы (h3O)x, где x — количество молекул. Наиболее энергетически выгодно объединение из пяти молекул воды (x = 5) с четырьмя водородными связями, в котором связи образуют равновесный, так называемый тетраэдральный угол, равный 109,47 градуса (см. рис. 2).
Проанализировав зависимость длины водородной связи между молекулами воды от температуры, Мацумото пришел к ожидаемому выводу: рост температуры рождает линейное удлинение водородных связей. А это, в свою очередь, приводит к увеличению объема воды, то есть к ее расширению. Сей факт противоречит наблюдаемым результатам, поэтому далее он рассмотрел влияние второго фактора. Как коэффициент теплового расширения зависит от топологического индекса?
Компьютерное моделирование дало следующий результат. При низких температурах наибольший объем воды в процентном отношении занимают кластеры воды, у которых на одну молекулу приходится 4 водородных связи (топологический индекс равен 4). Повышение температуры вызывает уменьшение количества ассоциатов с индексом 4, но при этом начинает возрастать число кластеров с индексами 3 и 5. Проведя численные расчеты, Мацумото обнаружил, что локальный объем кластеров с топологическим индексом 4 с повышением температуры практически не меняется, а изменение суммарного объема ассоциатов с индексами 3 и 5 при любой температуре взаимно компенсирует друг друга. Следовательно, изменение температуры не меняет общий объем воды, а значит, и топологический индекс никакого воздействия на сжатие воды при ее нагревании не оказывает.
Остается выяснить влияние углового искажения водородных связей. И вот здесь начинается самое интересное и важное. Как было сказано выше, молекулы воды стремятся объединиться так, чтобы угол между водородными связями был тетраэдральным. Однако тепловые колебания молекул воды и взаимодействия с другими молекулами, не входящими в кластер, не дают им этого сделать, отклоняя величину угла водородной связи от равновесного значения 109,47 градуса. Чтобы как-то количественно охарактеризовать этот процесс угловой деформации, Мацумото с коллегами, основываясь на своей предыдущей работе Topological building blocks of hydrogen bond network in water, опубликованной в 2007 году в Journal of Chemical Physics, выдвинули гипотезу о существовании в воде трехмерных микроструктур, напоминающих выпуклые полые многогранники. Позднее, в следующих публикациях, такие микроструктуры они назвали витритами (рис. 3). В них вершинами являются молекулы воды, роль ребер играют водородные связи, а угол между водородными связями — это угол между ребрами в витрите.
Согласно теории Мацумото, существует огромное разнообразие форм витритов, которые, как мозаичные элементы, составляют большую часть структуры воды и которые при этом равномерно заполняют весь ее объем.
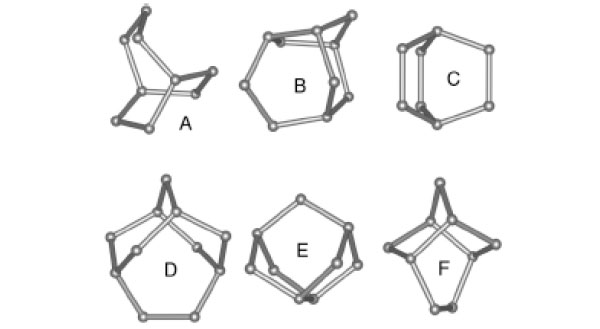
Молекулы воды стремятся создать в витритах тетраэдральные углы, поскольку витриты должны обладать минимально возможной энергией. Однако из-за тепловых движений и локальных взаимодействий с другими витритами некоторые микроструктуры не обладают геометрией с тетраэдральными углами (или углами, близкими к этому значению). Они принимают такие структурно неравновесные конфигурации (не являющиеся для них самыми выгодными с энергетической точки зрения), которые позволяют всему «семейству» витритов в целом получить наименьшее значение энергии среди возможных. Такие витриты, то есть витриты, которые как бы приносят себя в жертву «общим энергетическим интересам», называются фрустрированными. Если у нефрустрированных витритов объем полости максимален при данной температуре, то фрустрированные витриты, напротив, обладают минимально возможным объемом.
Компьютерное моделирование, проведенное Мацумото, показало, что средний объем полостей витритов с ростом температуры линейным образом уменьшается. При этом фрустрированные витриты значительно уменьшают свой объем, тогда как объем полости нефрустрированных витритов почти не меняется.
Итак, сжатие воды при увеличении температуры вызвано двумя конкурирующими эффектами — удлинением водородных связей, которое приводит к увеличению объема воды, и уменьшением объема полостей фрустрированных витритов. На температурном отрезке от от 0 до 4°C последнее явление, как показали расчеты, преобладает, что в итоге и приводит к наблюдаемому сжатию воды при повышении температуры.
Осталось дождаться экспериментального подтверждения существования витритов и такого их поведения. Но это, увы, очень непростая задача.
Источник: Masakazu Matsumoto. Why Does Water Expand When It Cools? // Phys. Rev. Lett. 103, 017801 (2009).
Юрий Ерин
elementy.ru
Новая теория, почему вода при нагревании от 0 до 4°C сжимается
Японский физик Масакадзу Мацумото выдвинул теорию, которая объясняет, почему вода при нагревании от 0 до 4°C сжимается, вместо того чтобы расширяться. Согласно его модели, вода содержит микрообразования — «витриты», представляющие собой выпуклые пустотелые многогранники, в вершинах которых находятся молекулы воды, а ребрами служат водородные связи. При повышении температуры конкурируют между собой два явления: удлинение водородных связей между молекулами воды и деформация витритов, приводящая к уменьшению их полостей. В диапазоне температур от 0 до 3,98°C последнее явление доминирует над эффектом удлинения водородных связей, что в итоге и дает наблюдаемое сжатие воды. Экспериментального подтверждения модели Мацумото пока что нет — впрочем, как и других теорий, объясняющих сжатие воды.
В отличие от подавляющего большинства веществ, вода при нагревании способна уменьшать свой объем (рис. 1), то есть обладает отрицательным коэффициентом теплового расширения. Впрочем, речь идет не обо всём температурном интервале, где вода существует в жидком состоянии, а лишь об узком участке — от 0°C примерно до 4°C. При больших температурах вода, как и другие вещества, расширяется.
Между прочим, вода — не единственное вещество, имеющее свойство сжиматься при увеличении температуры (или расширяться при охлаждении). Подобным поведением могут «похвастать» еще висмут, галлий, кремний и сурьма. Тем не менее, в силу своей более сложной внутренней структуры, а также распространенности и важности в разнообразных процессах, именно вода приковывает внимание ученых (см. Продолжается изучение структуры воды, «Элементы», 09.10.2006).
Некоторое время назад общепринятой теорией, отвечающей на вопрос, почему вода увеличивает свой объем при понижении температуры (рис. 1), была модель смеси двух компонент — «нормальной» и «льдоподобной». Впервые эта теория была предложена в XIX веке Гарольдом Витингом и позднее была развита и усовершенствована многими учеными. Сравнительно недавно в рамках обнаруженного полиморфизма воды теория Витинга была переосмыслена. Отныне считается, что в переохлажденной воде существует два типа льдообразных нанодоменов: области, похожие на аморфный лед высокой и низкой плотности. Нагревание переохлажденной воды приводит к плавлению этих наноструктур и к появлению двух видов воды: с большей и меньшей плотностью. Хитрая температурная конкуренция между двумя «сортами» образовавшейся воды и порождает немонотонную зависимость плотности от температуры. Однако пока эта теория не подтверждена экспериментально.
С приведенным объяснением нужно быть осторожным. Не случайно здесь говорится лишь о структурах, которые напоминают аморфный лед. Дело в том, что наноскопические области аморфного льда и его макроскопические аналоги обладают разными физическими параметрами.
Японский физик Масакадзу Мацумото решил найти объяснение обсуждаемого здесь эффекта «с нуля», отбросив теорию двухкомпонентной смеси. Используя компьютерное моделирование, он рассмотрел физические свойства воды в широком диапазоне температур — от 200 до 360 К при нулевом давлении, чтобы в молекулярном масштабе выяснить истинные причины расширения воды при ее охлаждении. Его статья в журнале Physical Review Letters так и называется: Why Does Water Expand When It Cools? («Почему вода при охлаждении расширяется?»).
Изначально автор статьи задался вопросом: что влияет на коэффициент теплового расширения воды? Мацумото считает, что для этого достаточно выяснить влияние всего трех факторов: 1) изменения длины водородных связей между молекулами воды, 2) топологического индекса — числа связей на одну молекулу воды и 3) отклонения величины угла между связями от равновесного значения (углового искажения).
|
Перед тем как рассказать о результатах, полученных японским физиком, сделаем важные замечания и разъяснения по поводу вышеупомянутых трех факторов. Прежде всего, привычная химическая формула воды h3O соответствует лишь парообразному ее состоянию. В жидкой форме молекулы воды посредством водородной связи объединяются в группы (h3O)x, где x — количество молекул. Наиболее энергетически выгодно объединение из пяти молекул воды (x = 5) с четырьмя водородными связями, в котором связи образуют равновесный, так называемый тетраэдральный угол, равный 109,47 градуса (см. рис. 2).
Проанализировав зависимость длины водородной связи между молекулами воды от температуры, Мацумото пришел к ожидаемому выводу: рост температуры рождает линейное удлинение водородных связей. А это, в свою очередь, приводит к увеличению объема воды, то есть к ее расширению. Сей факт противоречит наблюдаемым результатам, поэтому далее он рассмотрел влияние второго фактора. Как коэффициент теплового расширения зависит от топологического индекса?
Компьютерное моделирование дало следующий результат. При низких температурах наибольший объем воды в процентном отношении занимают кластеры воды, у которых на одну молекулу приходится 4 водородных связи (топологический индекс равен 4). Повышение температуры вызывает уменьшение количества ассоциатов с индексом 4, но при этом начинает возрастать число кластеров с индексами 3 и 5. Проведя численные расчеты, Мацумото обнаружил, что локальный объем кластеров с топологическим индексом 4 с повышением температуры практически не меняется, а изменение суммарного объема ассоциатов с индексами 3 и 5 при любой температуре взаимно компенсирует друг друга. Следовательно, изменение температуры не меняет общий объем воды, а значит, и топологический индекс никакого воздействия на сжатие воды при ее нагревании не оказывает.
Остается выяснить влияние углового искажения водородных связей. И вот здесь начинается самое интересное и важное. Как было сказано выше, молекулы воды стремятся объединиться так, чтобы угол между водородными связями был тетраэдральным. Однако тепловые колебания молекул воды и взаимодействия с другими молекулами, не входящими в кластер, не дают им этого сделать, отклоняя величину угла водородной связи от равновесного значения 109,47 градуса. Чтобы как-то количественно охарактеризовать этот процесс угловой деформации, Мацумото с коллегами, основываясь на своей предыдущей работе Topological building blocks of hydrogen bond network in water, опубликованной в 2007 году в Journal of Chemical Physics, выдвинули гипотезу о существовании в воде трехмерных микроструктур, напоминающих выпуклые полые многогранники. Позднее, в следующих публикациях, такие микроструктуры они назвали витритами (рис. 3). В них вершинами являются молекулы воды, роль ребер играют водородные связи, а угол между водородными связями — это угол между ребрами в витрите.
Согласно теории Мацумото, существует огромное разнообразие форм витритов, которые, как мозаичные элементы, составляют большую часть структуры воды и которые при этом равномерно заполняют весь ее объем.
|
Молекулы воды стремятся создать в витритах тетраэдральные углы, поскольку витриты должны обладать минимально возможной энергией. Однако из-за тепловых движений и локальных взаимодействий с другими витритами некоторые микроструктуры не обладают геометрией с тетраэдральными углами (или углами, близкими к этому значению). Они принимают такие структурно неравновесные конфигурации (не являющиеся для них самыми выгодными с энергетической точки зрения), которые позволяют всему «семейству» витритов в целом получить наименьшее значение энергии среди возможных. Такие витриты, то есть витриты, которые как бы приносят себя в жертву «общим энергетическим интересам», называются фрустрированными. Если у нефрустрированных витритов объем полости максимален при данной температуре, то фрустрированные витриты, напротив, обладают минимально возможным объемом.
Компьютерное моделирование, проведенное Мацумото, показало, что средний объем полостей витритов с ростом температуры линейным образом уменьшается. При этом фрустрированные витриты значительно уменьшают свой объем, тогда как объем полости нефрустрированных витритов почти не меняется.
Итак, сжатие воды при увеличении температуры вызвано двумя конкурирующими эффектами — удлинением водородных связей, которое приводит к увеличению объема воды, и уменьшением объема полостей фрустрированных витритов. На температурном отрезке от от 0 до 4°C последнее явление, как показали расчеты, преобладает, что в итоге и приводит к наблюдаемому сжатию воды при повышении температуры.
Осталось дождаться экспериментального подтверждения существования витритов и такого их поведения. Но это, увы, очень непростая задача.
Источник: Masakazu Matsumoto. Why Does Water Expand When It Cools? // Phys. Rev. Lett. 103, 017801 (2009).
Юрий Ерин
elementy.ru/news/431131
www.o8ode.ru
Вода как теплоноситель — ТеплоВики
Материал из ТеплоВики - энциклопедия отоплении
Наиболее важными свойствами воды являются:
Физические свойства воды
Удельная теплоемкость
Важным свойством любого теплоносителя является его теплоёмкость. Если выразить ее через массу и разность температур теплоносителя, то получится удельная теплоёмкость.
Она обозначается буквой c и имеет размерность кДж/(кг • K)
Удельная теплоемкость — это количество тепла, которое необходимо передать 1 кг вещества (например, воды), чтобы нагреть его на 1 °C. И наоборот, вещество отдает такое же количество энергии при охлаждении.
Среднее значение удельной теплоемкости воды в диапазоне между 0 °C и 100 °C составляет:
c = 4,19 кДж/(кг • K) или c = 1,16 Втч/(кг • K)
Количество поглощаемого или выделяемого тепла Q, выраженное в Дж или кДж, зависит от массы m, выраженной в кг, удельной теплоемкости c и разности температур, выраженной в K.
В системах отопления — это разность температур в прямом и обратном трубопроводе. Полученная формула:
Q = m • c • Δϑ m= V • ρ
V = Объем воды в м3 ρ = Плотность в кг/м3
Масса m — это объем воды V, выраженный в м3, умноженный на плотность ρ воды, выраженную в кг/м3. Таким образом, формулу можно представить в следующем виде:
Q = V • ρ • c ( ϑV - ϑR)
Известно, что плотность воды меняется в зависимости от ее температуры. Однако, чтобы упростить расчеты, используется = 1 кг/дм3 в диапазоне от 4 °C до 90 °C.
Физические термины "энергия", "работа" и "количество тепла" эквивалентны.
Следующая формула используется для преобразования джоулей в другие размерности:
1 Дж = 1 Нм = 1 Втс или 1 МДж = 0,278 кВтч
Увеличение и уменьшение объема
 Изменение объема воды
Изменение объема воды  Когда вода нагревается или охлаждается, ее плотность уменьшается.
Когда вода нагревается или охлаждается, ее плотность уменьшается. Все природные материалы расширяются при нагревании и сжимаются при охлаждении. Единственным исключением из этого правила является вода. Это уникальное ее свойство называется аномалией воды.
Вода имеет наибольшую плотность при +4 °C, при которой 1 дм3 = 1 л имеет массу 1 кг. Если вода нагревается или охлаждается относительно этой точки, ее объем увеличивается, что означает уменьшение плотности, т. е. вода становится легче.
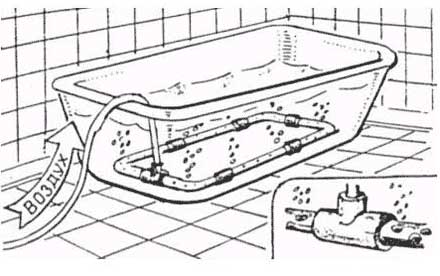
Это можно отчетливо наблюдать на примере резервуара с точкой перелива.
В резервуаре находится ровно 1000 см3 воды с температурой +4 °C. При нагревании воды некоторое количество выльется из резервуара в мерную емкость. Если нагреть воду до 90 °C, в мерную емкость выльется ровно 35,95 см3, что соответствует 34,7 г.
Характеристики кипения воды
 Изменение агрегатного состояния при повышении температуры
Изменение агрегатного состояния при повышении температуры Если воду нагревать в открытой емкости, она закипит при температуре 100 °C. Если измерять температуру кипящей воды, окажется, что она остается равной 100 °C пока не испарится последняя капля. Таким образом, постоянное потребление тепла используется для полного испарения воды, т. е. изменения ее агрегатного состояния. Эта энергия также называется латентной (скрытой) теплотой. Если подача тепла продолжается, температура образовавшегося пара снова начнет подниматься.
Описанный процесс приведен при давлении воздуха 101,3 кПа у поверхности воды. При любом другом давлении воздуха точка кипения воды сдвигается от 100 °C.
Если бы мы повторили описанный эксперимент на высоте 3000 м. — мы бы обнаружили, что вода там закипает уже при 90 °C. Причиной такого поведения является понижение атмосферного давления с высотой.
Чем ниже давление на поверхности воды, тем ниже будет температура кипения. И наоборот, температура кипения будет выше при повышении давления на поверхности воды. Это свойство используется, например, в скороварках.
График справа показывает зависимость температуры кипения воды от давления.
 Температура кипения воды как функция давления
Температура кипения воды как функция давления Давление в системах отопления намеренно повышается. Это помогает предотвратить образование пузырьков газа в критических рабочих режимах, а также предотвращает попадание наружного воздуха в систему.
Расширение воды при нагревании и защита от избыточного давления
Системы водяного отопления работают при температурах воды до 90 °C. Обычно система заполняется водой при температуре 15 °C, которая затем расширяется при нагревании. Нельзя допустить, чтобы это увеличение объема привело к возникновению избыточного давления и переливу жидкости.
 Система отопления со встроенным предохранительным клапаном
Система отопления со встроенным предохранительным клапаном Когда отопление отключается в летний период, объем воды возвращается к первоначальному значению. Таким образом, для обеспечения беспрепятственного расширения воды необходимо установить достаточно большой бак. Старые системы отопления имели открытые расширительные баки. Они всегда располагались выше самого высокого участка трубопровода. При повышении температуры в системе, что приводило к расширению воды, уровень в баке также повышался. При снижении температуры он, соответственно, понижался.
Современные системы отопления используют мембранные расширительные баки (МРБ).
При повышении давления в системе нельзя допускать увеличения давления в трубопроводах и других элементах системы выше предельного значения. Поэтому обязательным условием для каждой системы отопления является наличие предохранительного клапана.
При повышении давления сверх нормы предохранительный клапан должен открываться и стравливать лишний объем воды, который не может вместить расширительный бак. Тем не менее, в тщательно спроектированной и обслуживаемой системе такое критическое состояние никогда не должно возникать.
Все эти рассуждения не учитывают тот факт, что циркуляционный насос еще больше увеличивает давление в системе.
Взаимосвязь между максимальной температурой воды, выбранным насосом, размером расширительного бака и давлением срабатывания предохранительного клапана должна быть установлена самым тщательным образом. Случайный выбор элементов системы — даже на основании их стоимости — в данном случае неприемлем.
Мембранный расширительный бак поставляется заполненным азотом. Начальное давление в расширительном мембранном баке должно быть отрегулировано в зависимости от системы отопления. Расширяющаяся вода из системы отопления поступает в бак и сжимает газовую камеру через диафрагму. Газы могут сжиматься, а жидкости — нет.
Компенсация изменения объема воды в системе отопления:
 До заполнения системы водой
До заполнения системы водой  Система заполнена холодной водой
Система заполнена холодной водой  Система при макс. температуре воды
Система при макс. температуре воды Давление
Определение давления Давление — это статическое давление жидкостей и газов, измеренное в сосудах, трубопроводах относительно атмосферного давления (Па, мбар, бар).
Статическое давление Статическое давление — это давление неподвижной жидкости. Статическое давление = уровень выше соответствующей точки измерения + начальное давление в расширительном баке.
Динамическое давление Динамическое давление — это давление движущегося потока жидкости.
Давление нагнетания насоса Это давление на выходе центробежного насоса во время его работы.
Перепад давления Давление, развиваемое центробежным насосом для преодоления общего сопротивления системы. Оно измеряется между входом и выходом центробежного насоса.
Рабочее давление Давление, имеющееся в системе при работе насоса.
Допустимое рабочее давление Максимальное значение рабочего давления, допускаемого из условий безопасности работы насоса и системы.
Кавитация
Кавитация — это образование пузырьков газа в результате появления локального давления ниже давления парообразования перекачиваемой жидкости на входе рабочего колеса. Это приводит к снижению производительности (напора) и КПД и вызывает шумы и разрушение материала внутренних деталей насоса.
Из-за схлопывания пузырьков воздуха в областях с более высоким давлением (например, на выходе рабочего колеса) микроскопические взрывы вызывают скачки давления, которые могут повредить или разрушить гидравлическую систему. Первым признаком этого служит шум в рабочем колесе и его эрозия.
Важным параметром центробежного насоса является NPSH (высота столба жидкости над всасывающим патрубком насоса). Он определяет минимальное давление на входе насоса, требуемое данным типом насоса для работы без кавитации, т. е. дополнительное давление, необходимое для предотвращения появления пузырьков.
На значение NPSH влияют тип рабочего колеса и частота вращения насоса. Внешними факторами, влияющими на данный параметр, являются температура жидкости, атмосферное давление.
Предотвращение кавитации Чтобы избежать кавитации, жидкость должна поступать на вход центробежного насоса при определенной минимальной высоте всасывания, которая зависит от температуры и атмосферного давления.
Другими способами предотвращения кавитации являются:
- Повышение статического давления
- Понижение температуры жидкости (снижение давления парообразования PD)
- Выбор насоса с меньшим значением постоянного гидростатического напора (минимальная высота всасывания, NPSH)
ru.teplowiki.org
Нагревание водой - Справочник химика 21
Умягчение воды, т. е. удаление ионов кальция и магния, проводят термическим и химическим методами. Термическим методом разлагают бикарбонаты при нагревании воды до кипения. При химическом методе катионы кальция и магния замещают катионами натрия, водорода или аммония, которые не образуют накипи. Растворенные газы удаляют при кипячении воды в деаэраторе. [c.131] Присутствующие в йоде примеси хлора и брома, взаимодействуя с йодистым калием, образуют нелетучие хлористые и бромистые соли калия. Смесь йода с йодистым калием помещают в чистый стаканчик на стаканчик устанавливают небольшой кристаллизатор, в который наливают холодную воду дно кристаллизатора должно быть абсолютно чистым. Затем стаканчик с кристаллизатором помещают в песочную баню, которую нагревают на слабом пламени. При этом йод быстро возгоняется и осаждается на дне холодного кристаллизатора. По мере нагревания воды в кристаллизаторе ее заменяют холодной. При соблюдении указанных условий йод возгоняется в виде крупных кристаллов, легко отстающих от дна кристаллизатора. [c.131]Горячую воду получают в водогрейных котлах, обогреваемых топочными газами, и паровых водонагревателях (бойлерах). Она применяется обычно для нагрева до температур не более 100 С. Для температур выше 100 "С в качестве теплоносителя используют воду, находящуюся под избыточным давлением. Для нагревания водой применяют главным образом циркуляционные системы обогрева, которые описаны ниже. [c.313]
Даже в 1770 г. ряд ученых придерживались старого определения элементов и утверждали, что трансмутация возможна, поскольку воду, например, при длительном нагревании можно превратить в землю. Предположение о возможности превращения воды в землю считалось справедливым (вначале даже самим Лавуазье), так как при длительном нагревании воды (в течение нескольких дней) в стеклянном сосуде образовывался твердый осадок. [c.45]
Решение. Скорость выделения тепла в ходе реакции равна скорости нагревания воды, а также скорости теплопередачи. Таким образом [c.109]
При нагревании воды непосредственно в промывалке пробку с трубками нужно приподнять так, чтобы пробка не сидела плотно в горле колбы. Несоблюдение этого может привести к несчастному случаю в результате выбрасывания кипящей воды из капиллярного конца трубки. [c.31]
Расход теплоты из аппарата происходит за счет нагревания воды [c.49]
Падающий с известной высоты груз вращает мешалку, погруженную в воду, находящуюся в калориметре. (Груз и калориметр с водой составляют термодинамическую систему.) Вращение лопастей мешалки в воде вызывает нагревание воды в калориметре соответствующее повышение температуры количественно фиксируется. [c.29]
При нагревании воды с 25 до 40° С ее потребуется [c.232]
При нагревании воды (особенно озерной или речной) до 90—95 °С происходит интенсивное образование бурых хлопьев. Объясните это явление. Почему такое явление не наблюдается при нагревании дистиллированной воды [c.217]
Суш ность обработки заключается в вытеснении воды из пор гидрогеля и заменой ее молекулами вытеснителя. Известно, что высокомолекулярные соединения обладают более высокой адсорбируемостью. Процесс вытеснения воды ускоряется при нагревании вода в порах расширяется, давит на стенки нор, в то время как скелет гидрогеля при потере влаги сжимается. В результате смешения мокрого гидрогеля, прошедшего синерезис, активацию п промывку, с высококипящими нефтяными углеводородами свободные от воды поры заполняются молекулами вытеснителя, которые в дальнейшем не дают им возможности сжиматься. Углеводородные молекулы из-за их высокой температуры кипения в процессе обработки остаются в порах гидрогеля и удаляются из них только путем выжигания - последующим прокаливанием при 550—600 С. После выжигания вытеснителя норы силикагеля остаются свободными. Количество пор обусловливает величину адсорбирующей новерхности силикагеля, а от их размеров зависит степень избирательной активности по отношению к разным парам и газам. [c.118]
При обезвоживании нефти с применением нагревания возрастают также эксплуатационные расходы. Нагревание водо-нефтяной эмульсии по мере роста ее обводненности требует все больших затрат тепла, так как теплоемкость пластовой воды в два раза превышает теплоемкость нефти. Процесс обезвоживания нефти при повышенной температуре, для исключения газовыделения в дегидрирующей аппаратуре проводится под давлением, что значительно увеличивает расход электроэнергии. Кроме того, теплохимические установки требуют значительных эксплуатационных затрат, связанных со сложностью их обслужи-вания. [c.67]
Поскольку при добавлении тепла происходит медленное разрушение связанных водородной связью кластеров HjO, вода имеет большую теплоемкость, чем многие из других распространенных жидкостей, за исключением аммиака. Кроме того, вода имеет необычно высокую теплоту плавления и теплоту испарения. Совокупность этих трех свойств делает воду эффективным термостатом, который поддерживает температуру на поверхности Земли в умеренных пределах. При плавлении льда поглощается огромная энергия, а нагревание воды на каждый градус требует большей затраты тепла, чем для большинства других веществ. Соответственно при охлаждении воды она выделяет в окружающую среду больше тепла, чем многие другие вещества. [c.621]
Превращение поверхностных слоев многих окислов в поверхностные слои гидроокиси является результатом хемосорбции воды ча этих окислах. При нагревании вода десорбируется, а группы ОН снова переходят в ионы кислорода. [c.73]
На высокопроизводительных установках тепло отходящих дымовых газов используется для нагревания воды и производства водяного пара, что частично покрывает потребности в паре самой установки. [c.82]
Помимо хлоридов пластовые воды могут содержать значительное количество бикарбонатов кальция и магния, которые часто называют солями временной жесткости. Это название обусловлено следующим. В результате нагревания воды, смешения ее со щелочной водой и других причин эти соли могут разлагаться по схеме [c.10]
Устройства, предназначенные для получения водяного пара или нагревания воды, называются котельными установками. Различают паровые и водогрейные котельные установки. По назначе- [c.125]
Необходимое для нагревания воды количество пара О равно [c.122]
Устройства, которые служат для непосредственной выработки пара и нагревания воды, называются паровыми или водогрейными котлами. [c.127]
При других значениях Дпаровых змеевиков в случае нагревания воды приведенные значения й следует умножать на коэффициент, [c.586]
Обычно этот способ применяют для нагревания воды п водных растворов. [c.161]
Постоянная (некарбонатная) жесткость обусловлена присутствием таких растворимых солей кальция и магния, как сульфаты, хлориды, нитраты и др. Они при нагревании воды не разрушаются. Сумма карбонатной и [c.71]
В результате до 70% металлоемкости термохимических установок, до 50% капитальных затрат и эксплуатационных расходов на подготовку нефти связаны с необходимостью нагревания водо-нефтяной эмульсии. [c.67]
Пример V. 3. Определить а) температуру нагревания воды при растворении безводного едкого кали в количестве, необходимом для образования 15%-ного раствора [c.118]
Из уравнения теплового баланса определяем время нагревания воды до заданной температуры [c.122]
Парообразователь служит источником пара для перегонки с водяным паром и для нагрева водяных бань. Он представляет собой металлический сосуд (чаще всего — медный) со стеклянной трубкой, опущенной почти до дна. Эта трубка предохраняет от резкого повышения давления при сильном нагревании воды (рис, 8). [c.19]
Т[1ебуется нагреть 5 л поды от температуры 20° до 100° С при помощи гока силой в 4 и. В качестве нагревателя служит обмотка из нихромовой проволоки, длина которой 2. и и сопротивление 65 ом1м. Сколько потребуется времени на нагревание воды (тепловыми потерями в окружающую сряду пренебречь) [c.262]
При нагревании воды продолжается разрыв водородных связей, что приводит к уменьшению объема воды и повышению ее плотности. В интервале температур от О до 4 "С этот эффект преобладает над тепловьи. г pa ninpeiMieM, так что плотность БОДЫ продолжает возрастать. Однако нри нагревании вЕЛ[не 4 °С преобладает влияние усиления тен-лопого движения мплекудг и плотность поды уменьшается. Поэтому при 4 °С вода обладает максимальной п,/ютностью. [c.208]
При нагревании воды часть теплоты затрачивается на разрыв водородных связей (энергия разрыва водородной связи в воде составляет примерно 25 кДж/моль). Этим объясняется высо1 ая теплоем1сость воды. [c.208]
Успех описываемого процесса был обусловлен не только упрощением стадии разделения продуктов, но и эффективной системой утилизации тепла. Остаточный воздух вместе с парами органических неществ с верха реактора поступает в котел-утилизатор 3, где генерируется пар соответствующего давления. Тепло газа используют затем в теплообменнике 4 для нагревания воды, а давление газа п детандере 6 преобразуют в холод, при помощи которого в xoлoдиJ[ыяикe 5 из газа конденсируют остатки унесенного им бензина. Объединенный конденсат возвращают в колонну окисления. [c.381]
Метод азеотропной дистилляции, или, как его часто называют, метод Дина и Старка (ГОСТ 2477—65). Относится к прямым методам измерений. Принципиальная схема прибора, применяемого для этого метода, представлена на рис. 9.2. Пробу нефти заливают в колбу 1 и к ней добавляют осушенный растворитель — обычно бензин Галоша . В колбу вставляют водоловушку 2 с обратным холодильником 3. Все это устанавливают на нагреватель 4. В процессе нагревания вода в парообразном состоянии вместе с растворителем попадает в обратный холодильник 3. В нем пары воды и растворителя конденсируются и стекают в ловушку 2, где и разделяются на два слоя за счет разности плотностей. Избыток растворителя возвращается из ловушки в колбу [c.164]
Взрыв железнодорожной цистерны, содержавшей жидкий фосфор, произошел 4 февраля 1978 г. в Браунсоне (шт. Небраска, США). Эта авария описана в работе [Hymes,1985]. Причиной взрыва послужил сход с рельсов товарного поезда, в составе которого был 31 вагон с различными грузами. Цистерна, содержавшая фосфор, перевернулась и лежала под углом 15° к горизонту. Сверху на цистерну упали еще три вагона. Началась утечка жидкого фосфора. Пожарные соорудили вокруг цистерны обвалование, чтобы фосфор не растекался. Фосфор воспламенился, над местом пожара поднимались клубы белого дыма - это был пентаоксид фосфора, вещество средней токсичности. Через 7 ч цистерна взорвалась. Силой взрыва горящий фосфор был разбросан по территории площадью 0,15 км , в результате чего несколько человек получили ожоги различной степени тяжести (вплоть до третьей). Другие в результате взрыва получили механические травмы. В цитируемой работе высказано несколько предположений о природе взрыва, но указывается, что наиболее правдоподобной выглядит гипотеза, согласно которой взрыв произошел от нагревания воды, находившейся внутри цистерны (фосфор перевозили под слоем воды), до 250 °С. Такой температуре соответствует давление внутри резервуара 3,8 МПа, - вполне достаточное, чтобы разорвать оболочку цистерны. [c.449]
По практическим данным, для паровых змеевиков при нагревании воды начальная скорость пара в змеевике не должна превышать 30 uj eK. Предельное наибольшее отношение Ijd (где i — длина каждого змеевика), в зависимости от абсолютного давления пара р при средней разности температур Д/ср = = 30-f-40 град, составляет [VII-6] [c.586]
В установках с естественной циркуляцией в качестве теплопоси-геля обычно применяют перегретую воду или высокотемпературные органические теплоносители. Максимальная темнература нагревания воды равна ее критической темпе])атуре 374° С нри соответствуюш,ем абсолютном давлении 225 ат. До герметизации циркуляционной системы при разогреве из цее должен быть удален воздух или другие неконденсируюш,иеся газы, поэтому установку заполняют только дистиллированной водой. [c.168]
Анализ затрат на обезвоживание нефти на промысловых установках, работающих по термохимической схеме, показывает, что необходимость нагревания водо-нефтяной эмульоии значительно увеличивает капитальные и эксплуатационные затраты на подготовку нефти, часто превышающие затраты на перекачку нефти на значительные расстояния с повышенной обводненностью. Осуществление обезвоживания нефти с применением нагревания вызывает не-обходи,мость включения в ко мплекс сооружений установок подготовки нефти котельных или огневых печей, монтажа большого количества теплообменной аппаратуры и запорной арматуры, что значительно увеличивает металлоемкость установок и капитальные затраты на их строительство. [c.67]
В последнее время все большее применение в качестве адсорбентов и катализаторов находят цеолиты, как природные, так и синтетические. Цеолиты — это алюмосиликаты, обладающие строго регулярной кристаллической структурой. Каркас кристалла цеолита состоит из структурных тетраэдрических элементов 8104 и А1О4 , соединенных между собой общими атомами кислорода. Отрицательный заряд каркаса благодаря наличию в нем трехзарядного алюминия компенсируется зарядом катионов щелочных и щелочноземельных металлов, располагающихся в полостях структуры. В зависимости от кристаллической структуры окна этих полостей имеют размеры 0,4—1,1 нм (соизмеримые с размерами молекул). Поэтому на цеолитах могут адсорбироваться только те вещества, молекулы которых имеют размер по наименьшей оси (критический диаметр) меньше диаметра окна полости. Отсюда второе название цеолитов — молекулярные сита. Цеолиты жадно поглощают воду, и поэтому широко применяются для осушки газовых и некоторых жидких сред. При нагревании вода из них испаряется, с чем и связано нх название — цеолиты (кипящий камень — кипеть, литое — камень). Цеолиты научились синтезировать совсем недавно (1948). Особенностью их синтеза является процесс кристаллизации после получения алюмосиликагеля. [c.130]
Процесс изобарного парообразования состоит из трех основных стадий нагревания воды до кипения, испарения воды при температуре кипения и нагревания образовавшегося сухого насыщенного пара до состояния перегретого пара. Теплота Qпap этого процесса может быть определена как сумма теплот нагр — нагревания воды до температуры кипения исп — изотермического испарения жидкости при температуре кипения с образованием сухого насыщенного пара и Спер — нагревания полученного сухого насыщенного пара до заданного состояния перегретого пара. Однако при использовании скелетных таблиц и тепловых диаграмм эта операция сводится к определению разности энтальпии Япер перегретого пара и энтальпии Яв1 воды в ее исходном состоянии [c.78]
chem21.info