Почему введен запрет на свободную продажу Марганцовки. Почему марганцовка в воде желтеет
Запрещена Марганцовка в аптеках? Чем заменить Марганцовку
 Калия перманганат, а в народе марганцовка, представляет собой маленькие кристаллы насыщенного фиолетового оттенка с характерным металлическим отблеском. Препарат хорошо растворяется в воде, цвет которой приобретает насыщенный розовый или темно-фиолетовый оттенок, в зависимости от концентрации вещества в жидкости.
Калия перманганат, а в народе марганцовка, представляет собой маленькие кристаллы насыщенного фиолетового оттенка с характерным металлическим отблеском. Препарат хорошо растворяется в воде, цвет которой приобретает насыщенный розовый или темно-фиолетовый оттенок, в зависимости от концентрации вещества в жидкости.
Является антисептическим средством, которым еще буквально 5-10 лет тому назад пользовались практически в каждом доме. С помощью марганцовки можно делать слабый обеззараживающий раствор воды в ванной и купать в нем ребенка.
Очень слабый раствор вызывает рвоту, что поможет при отравлениях.
Перманганат калия отлично справляется с разного рода инфицированными ранами, которые долго не заживают, достаточно пару раз на день обрабатывать гнойные поражения кожи раствором, и они начнут быстрее заживать.
Полезна марганцовка и при ангине, с помощью нее можно бороться с вредоносными бактериями в горле – всего лишь нужно делать полоскания 3 раза в день. Также ею можно лечить молочницу влагалища, промывать ожоги на коже. С помощью рецептов народной медицины калия перманганатом можно лечить понос, гастрит и геморрой.
Подробная инструкция доступна по ссылке: http://lekhar.ru/lekarstva/antiseptiki/margancovka-instrukcija-po-primeneniju/
Не смотря на все полезные качества и явную пользу в быту, на данный момент марганцовка запрещена в России для свободной продажи. Тот, кто будет несанкционированно продавать калия перманганат, подлежит уголовному наказанию.
Почему нельзя купить марганцовку – основные причины
Существует 4 веские причины отсутствия данного препарата на аптечных прилавках:
- Из него могут делать бомбы и взрывоопасные вещества
- Наркозависимые используют кристаллы препарата в качестве одного из составных опаснейшего наркотического вещества – первитина
- Продавать калиевую соль марганцевой кислоты неудобно и невыгодно
- Марганцовка опасна для потребления – неверные дозировки могут вызвать отек и ожог гортани, ротовой полости
Пояснение касательно первого пункта – так как вещество действительно взрывоопасно, оно должно храниться в определенных условиях, этим могут похвастаться далеко не все аптеки в России. Если в аптечном помещении есть место для хранения кристаллов, которое пропитано огнеупорными веществами, то только тогда по закону оно может продаваться. Также нельзя выставлять этот медикамент на витрину прилавка.
Пояснение касательно второго пункта – наркотическое вещество под названием первитин наркозависимые научились делать из перманганата калия и бронхолитина (средство от кашля, в состав которого входит эфедрина гидрохлорид). В связи с этим властям пришлось внести изменения в список сильнодействующих наркотических веществ и внести туда калиевую соль марганцевой кислоты.
Пояснение насчет третьего пункта — если работник аптечного учреждения продает данный препарат, то он обязан вести строгий учет по продажам. Также по рецепту нельзя отпускать более двух бутылочек медикамента. Плюс ко всему марганцовка должна храниться в особых условиях, указанных в первом пункте (с противопожарной системой), а специально устанавливать огнеупорную защиту ради копеечного лекарства, которое продается в ограниченном количестве – вообще не выгодно. Вот почему препарат так сложно найти.
И наконец, последний пункт – калиевая соль марганцевой кислоты действительно представляет опасность для здоровья детей и невнимательных людей, которые не могут правильно рассчитать верную концентрацию средства для перорального употребления. Если человек выпил больше необходимого, медикамент легко спровоцирует ожог или отек. Случаи отравления перманганатом калия, когда он был в свободной продаже, встречались в медицинской практике часто, особенно среди несовершеннолетних.
Что делать, если ребенок выпил раствор или съел кристаллы?
Все зависит от количества выпитого или съеденного средства. Если ребенок выпил слабый раствор медикамента бледно-розового цвета, то с ним, скорее всего ничего не случится. В таком случае нужно, чтобы он выпил пол-литра или литр кипяченой теплой воды.  Далее надо постараться вызвать рвоту. Если же ребенок выпил темный раствор, то придется лечить отравление, потому что в большой концентрации может возникнуть отек гортани или ожог пищевода. Требуется немедленная госпитализация, чтобы в условиях стационара ребенку промыли желудок и начали лечить от повреждений желудка, если они есть. Хуже всего, если ребенок съел кристаллы, потому что это концентрированная форма. В таком случае сразу вызывается скорая помощь, делаются очистительные процедуры ЖКТ.
Далее надо постараться вызвать рвоту. Если же ребенок выпил темный раствор, то придется лечить отравление, потому что в большой концентрации может возникнуть отек гортани или ожог пищевода. Требуется немедленная госпитализация, чтобы в условиях стационара ребенку промыли желудок и начали лечить от повреждений желудка, если они есть. Хуже всего, если ребенок съел кристаллы, потому что это концентрированная форма. В таком случае сразу вызывается скорая помощь, делаются очистительные процедуры ЖКТ.
Скорее всего, придется лечить ребенка от последствий съеденного порошка. В самых тяжелых случаях придется делать операцию. Возможные последствия: в лучшем случае будет рвота и понос, а в худшем – ожог пищевода, отек гортани, судорожные припадки, геморрагический колит, нефропатия, гепатопатия.
Смертельная доза для ребенка считается 3 грамма вещества, а для взрослого колеблется от 0.3 до 0.5 грамм на килограмм веса. Также в домашних условиях, чтобы предотвратить ожог, можно дать выпить раствор соды. Так как перманганат калия – это не что иное, как калиевая соль марганцевой кислоты, а все кислоты нейтрализуются щелочью, то сода может сгладить возможные негативные последствия, если был выпит слабый раствор в небольшом количестве.
Почему марганцовка желтеет в воде?
На самом деле, многие люди задаются этим вопросом и не понимают что делать, когда видят такую странную реакцию. Если в проточной воде перманганат калия меняет розовый или фиолетовый цвет на желтый, это означает, что в воде содержатся продукты распада органических соединений, с которыми калиевая соль марганцевой кислоты вступает в реакцию, из-за чего образуется такой оттенок. Это свойство перманганата калия очень полезно в быту, так можно проверить качество питьевой воды: достаточно накапать пару капель раствора, и если он пожелтеет, значит, такую воду не стоит пить.
lekhar.ru
Почему марганцовка желтеет в воде?
Вернувшись домой из роддома, счастливые молодые родители впервые сталкиваются со множеством трудностей, и купание новорождённого — одна из них. Этот процесс осложняется незажившей ранкой на пупке, поэтому часто можно услышать о необходимости применения марганцовки. Но как её развести в воде и насколько она безвредна для малыша?
При купании новорождённого дома необходимо учитывать, что через незажившую пупочную ранку в организм крохи могут проникнуть болезнетворные бактерии или раздражающие вещества. Раньше всегда педиатры рекомендовали для снижения риска воду кипятить, но этот процесс очень трудоёмкий. И вот тут уместно вспомнить об антисептических средствах. Одно из них — марганцовка.
У многих возникает закономерный вопрос, а можно ли купать младенца в растворе перманганата калия, всё же это химическое вещество. Ответ: можно, если правильно им пользоваться.
Есть мнение, что ребёнка можно купать в воде с добавлением марганцовки. И это не лишено смысла, ведь именно марганцовокислый калий используют в медицине для обеззараживания и обработки кожных покровов.
Марганцовокислый калий продаётся в виде кристаллов. Если один из них попадёт на влажную кожу, то можно получить сильный ожог, потому что это вещество очень концентрированное.
Порошок марганцовки представляет собой концентрированные кристаллы химического вещества, которые необходимо разбавить в воде
Для того чтобы избежать подобного при купании новорождённого, порошок перманганата следует развести водой. Ни в коем случае нельзя насыпать его непосредственно в ванночку. При размешивании может случиться так, что не все комочки растворятся полностью и один из них соприкоснётся с кожей ребёнка. В этом случае ожог неизбежен.
Порядок добавления марганцовки в воду для купания таков:
- в стеклянную посуду, например, в банку, налить воду;
- в неё положить 5–7 кристаллов марганцовки;
- хорошо размешать до максимального растворения вещества. В результате вода окрасится в тёмно-бордовый цвет;
- взять другую посуду и покрыть её двойным слоем марли, можно даже уплотнить кусочком хлопчатобумажной ваты;
- через этот фильтр процедить тёмный раствор марганцовки, все нерастворенные комочки осядут на вате и не попадут во вторую ёмкость;
- в ванночку с водой налить немного раствора так, чтобы жидкость приобрела нежно-розовую окраску.
Вода с марганцовкой должна быть нежно-розового цвета, но ни в коем случае не темнее.
В зависимости от того, сколько добавить кристаллов марганцовки, готовый раствор окрашивается в разный цвет
Оглавление [Показать]Как правильно купать новорождённого в растворе перманганата
Купать ребёнка в растворе марганцовки нужно как в обычной воде, определённых правил для этого нет. Желательно, конечно, чтобы жидкость не попала в глаза или рот. Особого вреда это не принесёт, но может вызвать небольшое раздражение слизистой органа зрения или послабление стула, слабую тошноту. Это всё нежелательные явления.
Ещё одно правило — не следует купать ребёнка в марганцовке долго. Помимо дезинфицирующего действия, она вызывает сухость кожи. Именно поэтому водные процедуры в растворе перманганата калия не должны продолжаться более 10 минут.
Марганцовка — прекрасный вариант для тех, кто хочет обезопасить новорождённого от заражения. Этот раствор оказывает антисептическое действие на воду из-под крана, помогая решить вопрос её чистоты.
Купание новорождённого в растворе марганцовки ничем не отличается от купания в обычной воде
Благодаря свойству подсушивать и нейтрализовать бактерии, перманганат калия может помочь, если у ребёнка на коже есть сыпь, потница, раздражение, опрелости.
В последнее время всё чаще современные медики отвергают испытанные «бабушкины» способы ухода за младенцами. Под запрет попадают и дешёвые лекарства, и питание, и одежда, и средства гигиены. В том числе это коснулось и марганцовки. Недостатки её применения очевидны, но не так страшны, если соблюдать правила использования перманганата.
- Сухость кожи от купания в растворе марганцовки — это, безусловно, минус. Но в то же время это ускоряет процесс заживления пупочной ранки. Чтобы свести к минимуму данный нежелательный эффект, пользуйтесь детскими увлажняющими средствами после каждого купания.
- При неправильном приготовлении раствора есть риск получения ожогов кожи и слизистых оболочек, поэтому необходимо строго соблюдать все правила разведения вещества в воде.
- Окрашивание кожи в жёлтый цвет — побочный эффект, который возникает только при купании в концентрированном растворе, что запрещено делать в случае с новорождённым.
Все эти минусы находятся под контролем родителей: если они будут правильно использовать перманганат калия, то и негативных последствий не будет ни при каких условиях. И всё же не следует использовать марганцовку для купания, если у малыша есть открытые ранки, кожные покровы слишком сухие или замечена аллергия именно на раствор данного вещества.
В последнее время марганцовку перестали повсеместно продавать в аптеках. Её ликвидация из списка разрешённых к свободной реализации медикаментов связана с использованием вещества для приготовления наркотических средств. Но к вреду для здоровья при обычном её применении это не имеет никакого отношения.
Если родители приняли решение отказаться от купания ребёнка в растворе марганцовки, то средство легко можно заменить отварами трав, например, ромашкой, которая также оказывает слабое подсушивающее и антисептическое действие. Только сырьё нужно купить не в виде чайных пакетов, а в форме сушёных соцветий россыпью. Заварить необходимо согласно инструкции на упаковке.
Вместо раствора марганцовки, для купания ребёнка можно приготовить отвар или настой лекарственных трав
Если у малыша на коже есть сыпь от крапивницы, потница или другие мелкие раздражения, включая микротрещинки, можно использовать отвар череды или чистотела. При повышенной возбудимости допускается ванна с валерианой или мятой. В любом случае обязательно наблюдайте за реакцией ребёнка на добавки в воду для купания, ведь травяные настои могут вызывать аллергию.
Хорошо известный доктор Комаровский, однако, считает бесполезным применение марганцовки для купания младенцев. Он утверждает, что для полного обеззараживания воды раствор должен быть более концентрированным, нежели допускается специалистами. А если разбавлять его до слабо-розового цвета, то антисептическое действие сводится на нет. По его мнению, использование перманганата — это плюс на совести родителей, которые чрезмерно беспокоятся о своём малыше.
О купании новорождённого в марганцовке есть абсолютно противоположные мнения. По этому вопросу лучше проконсультироваться с педиатром. Многие врачи всё же рекомендуют первые две-три недели использовать перманганат. Родители должны знать, что вреда он не нанесёт, а пользу при известных симптомах оказать вполне способен.
Еще несколько лет назад в каждом доме был пузырек с фиолетовым кристаллами, в народе называемыми марганцовкой. Этот раствор использовался для разных целей. И многие помнят розовую, неприятную на вкус воду, которую приходилось пить при отравлениях или обрабатывать ей раны. Но в последние годы многие люди столкнулись с проблемой: невозможно приобрети этот препарат. И они в недоумении: почему запретили марганцовку? Ведь этот дешевый антисептик часто незаменим в быту и медицине.
Научное название этого препарата — перманганат калия. Он является самым популярным антисептиком для наружного и внутреннего применения. Свежий раствор марганцовки обладает окисляющими свойствами и способен убить большинство микробов. Как же применяется марганцовка?
— слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
— более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
— в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
— марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
— хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
— ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.
До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
При разведении препарата нужно внимательно следить, чтобы его кристаллы не попали на кожу и слизистые и полностью растворились в воде. Ведь они могут вызвать сильный ожог и раздражение кожи. Поэтому при приготовлении препарата рекомендуют сначала приготовить более концентрированный раствор, а потом уже его добавлять в воду. Особенно это важно при внутреннем применении марганцовки и при использовании ее для ванночек ребенку. Кроме того, перманганат калия является легковоспламеняющимся веществом, и может произойти взрыв при трении его кристаллов о железо или при нарушении условий хранения.
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
1. Соли калия очень нестабильны и при определенных условиях могут воспламеняться, вплоть до взрыва. Это может произойти даже при комнатной температуре и при несоблюдении условий хранения препарата. Этим свойством часто пользуются террористы при изготовлении взрывных устройств. Это одна из причин, почему запретили продажу марганцовки в больших количествах.
2. Кроме того, перманганат калия относится к средствам, которые называются «перекурсоры». Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Но как ни странно, официально реализация перманганата калия в аптеках не запрещена, а просто ограничена. Те, кто с возмущеньем интересуются, почему запретили продавать марганцовку, получают ответ, что купить ее все-таки можно. Продается препарат по рецепту врача или в небольшом количестве, по 1-2 пакетика в одни руки. Оказывается, на аптеки наложили строгие ограничения и ввели новые правила относительно хранения и продажи препарата. Во многих городах провизоров обязуют вести строгий учет прихода и расхода марганцовки. А сами аптеки должны быть оборудованы специально для безопасного хранения этого взрывоопасного препарата. Поэтому большинство хозяев аптечного бизнеса отказываются продавать такое «неудобное», к тому же недорогое лекарство. Потому приобрести марганцовку можно, но в немногих государственных учреждениях.
У некоторых в доме еще остались старые запасы такого нужного препарата. Но те, кто столкнулся с необходимостью купить новую упаковку этого антисептика, выясняют, что марганцовка запрещена. Почему? Люди в недоумении. Ведь существуют еще более опасные препараты и вещества, используемые для приготовления наркотиков. И в то же время они находятся в свободной продаже. Это например, ацетон или средство для прочистки труб «Крот». Для изготовления наркотических средств используется также дистиллированная вода, сахар, кофе и многие другие вещества. Но в ограниченной продаже оказалась только марганцовка. Почему запрещена, причины этого не могут внятно разъяснить ни в одной аптеке. Поэтому люди часто возмущаются. А то, что это пока еще не стало массовым процессом, можно объяснить запасами перманганата калия во многих домах.
Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
Реагенты
- Гидроксид кальция
- Перманганат калия
- Сульфат натрия
- Глицерин
Безопасность
-
Перед началом опыта наденьте защитные перчатки и очки.
-
Проводите эксперимент на подносе.
Общие правила безопасности
- Не допускайте попадания химических реагентов в глаза или рот.
- Не допускайте к месту проведения экспериментов людей без защитных очков, а также маленьких детей и животных.
- Храните экспериментальный набор в месте, недоступном для детей младше 12 лет.
- Помойте или очистите всё оборудование и оснастку после использования.
- Убедитесь, что все контейнеры с реагентами плотно закрыты и хранятся по правилам после использования.
- Убедитесь, что все одноразовые контейнеры правильно утилизированы.
- Используйте только оборудование и реактивы, поставляемые в наборе или рекомендуемые текущими инструкциями.
- Если вы использовали контейнер для еды или посуду для проведения экспериментов, немедленно выбросьте их. Они больше не пригодны для хранения пищи.
Информация о первой помощи
- В случае попадания реагентов в глаза тщательно промойте глаза водой, при необходимости держа глаз открытым. Немедленно обратитесь к врачу.
- В случае проглатывания промойте рот водой, выпейте немного чистой воды. Не вызывайте рвоту. Немедленно обратитесь к врачу.
- В случае вдыхания реагентов выведите пострадавшего на свежий воздух.
- В случае контакта с кожей или ожогов промывайте поврежденную зону большим количеством воды в течение 10 минут или дольше.
- В случае сомнений немедленно обратитесь к врачу. Возьмите с собой химический реагент и контейнер от него.
- В случае травм всегда обращайтесь к врачу.
Рекомендации для родителей
- Неправильное использование химических реагентов может вызвать травму и нанести вред здоровью. Проводите только указанные в инструкции эксперименты.
- Данный набор опытов предназначен только для детей 12 лет и старше.
- Способности детей существенно различаются даже внутри возрастной группы. Поэтому родители, проводящие эксперименты вместе с детьми, должны по своему усмотрению решить, какие опыты подходят для их детей и будут безопасны для них.
- Родители должны обсудить правила безопасности с ребенком или детьми перед началом проведения экспериментов. Особое внимание следует уделить безопасному обращению с кислотами, щелочами и горючими жидкостями.
- Перед началом экспериментов очистите место проведения опытов от предметов, которые могут вам помешать. Следует избегать хранения пищевых продуктов рядом с местом проведения опытов. Место проведения опытов должно хорошо вентилироваться и находиться близко к водопроводному крану или другому источнику воды. Для проведения экспериментов потребуется устойчивый стол.
- Вещества в одноразовой упаковке должны быть использованы полностью или утилизированы после проведения одного эксперимента, т.е. после открытия упаковки.
Другие эксперименты
Пошаговая инструкция
-
В пластиковую пробирку аккуратно высыпьте всё содержимое баночки с KMnO4 (200 мг смеси сульфата натрия Na2SO4 с KMnO4, 1% содержание по массе).
-
Вылейте в пробирку содержимое баночки с насыщенным раствором гидроксида кальция Ca(OH)2 (5 мл).
-
Плотно закройте пробирку крышкой и перемешайте. Убедитесь, что вы получили прозрачный раствор.
-
Добавьте к получившемуся фиолетовому раствору 2 капли 10%-го водного раствора глицерина.
-
Плотно закройте пробирку и встряхните её.
-
Внимательно следите за раствором в пробирке! Наблюдайте изменение цвета хамелеона.

Ожидаемый результат
Две капли глицерина превращают фиолетовый раствор перманганата калия KMnO4 сначала в зелёный, а затем — в оранжевый.
Утилизация
Утилизируйте твёрдые отходы эксперимента вместе с бытовым мусором. Слейте растворы в раковину, промойте избытком воды.
Что произошло
Почему марганцовка меняет цвет?
Марганцовкой называют раствор перманганата калия KMnO4. Он имеет насыщенный фиолетовый цвет. Однако после добавления глицерина в этот раствор мы наблюдаем достаточно быстрое изменение окраски: пробирка превращается в хамелеона. Что же происходит? В воде KMnO4 распадается на две заряженные частицы:
KMnO4 → K+ + MnO4-
Именно MnO4- отвечает за фиолетовое окрашивание раствора. Частица MnO4- взаимодействует с глицерином. Сначала получается зелёный MnO42-:
MnO4- → MnO42-;
а затем бурый MnO2:
MnO42 → MnO2.
Атом марганца Mn в KMnO4 имеет внушительный положительный заряд (+7). Mn+7 – это сильный окислитель, а значит, он очень хочет заполучить в своё владение электроны (e-). Обычно Mn+7 забирает себе сразу несколько электронов – так сильно он хочет ими «полакомиться». Однако условия нашей реакции подобраны так, чтобы «голодный» марганец не торопился и насыщался электронами постепенно. А глицерин выступает в роли заботливой домохозяйки, подающей марганцу электроны порция за порцией:
MnO4- + e- → MnO42-;
MnO42 + 2e- → MnO2;
MnO2 + 2e- → Mn2+.
Фиолетовый перманганат MnO4- (заряд марганца +7, Mn7+) получает электрон и становится зелёным манганатом MnO42- (заряд марганца +6, Mn6+). Глицерин «кормит» его двумя электронами, и манганат превращается в бурый диоксид марганца MnO2 (Mn4+). Диоксид марганца мог бы взять ещё два электрона и превратиться в бесцветный Mn2+. Однако в условиях нашей реакции MnO2 выпадает в осадок, и этого не происходит.
Реакции, в которых вещества обмениваются электронами, называются окислительно-восстановительными. Жадные до электронов атомы называются окислителями, а те из атомов, которые отдают свои электроны («кормят» окислителей), – восстановителями. В нашем случае марганец – это окислитель, а глицерин – восстановитель.
Кстати, заряды у атомов, (например: +1 у K+, +7 у Mn+7 или -1 у Cl-) химики называют степенями окисления. Подробнее о них вы можете прочитать в описании эксперимента «Исчезающий йод».
Если внимательно следить за хамелеоном, вы заметите, что через несколько секунд после добавления глицерина в раствор он приобретёт синюю окраску. Синий цвет образуется при смешении фиолетового (от перманганата MnO4-) и зелёного (от манганата MnO42-) растворов. Однако он достаточно быстро зеленеет – в растворе становится всё меньше MnO4- и больше MnO42-.
Учёным удалось обнаружить, в какой форме марганец способен окрашивать раствор в синий цвет. Это происходит, когда он образует гипоманганат-ион MnO43-. Здесь марганец находится в степени окисления +5 (Mn+5). Однако MnO43- очень неустойчив, и для его получения необходимы особые условия, поэтому в нашем опыте его увидеть не получится.
Глицерин взаимодействует с перманганатом калия, отдавая ему свои электроны. Глицерин взят в нашей реакции в большом избытке (его примерно в 10 раз больше, чем перманганата калия KMnO4). Сам глицерин в условиях нашей реакции превращается глицериновый альдегид, а затем − в глицериновую кислоту.
Как мы уже выяснили, глицерин C3H5(OH)3 окисляется перманганатом калия. Глицерин – это весьма сложная органическая молекула, поэтому и реакции с его участием зачастую непросты. Окисление глицерина – сложная реакция, в ходе которой образуется много различных веществ. Многие из них существуют совсем недолго и превращаются в другие, а некоторые можно найти в растворе и после окончания реакции. Такая ситуация характерна для всей органической химии в целом. Обычно те вещества, которых по итогам химической реакции получается больше всего, называют основными продуктами, а остальные – побочными.
В нашем случае основной продукт окисления глицерина перманганатом калия – это глицериновая кислота.
В водном растворе гидроксид кальция Ca(OH)2 распадается на три заряженные частицы (ионы):
Ca(OH)2 → Ca2+(раствор) + 2OH-.
В транспорте, магазине, кафе или в школьном классе – везде нас окружают разные люди. И ведём мы себя в таких местах по-разному. Даже если делаем одно и то же дело – например, читаем книгу. В окружении разных людей мы делаем это немного по-разному: где-то медленнее, где-то быстрее, иногда запоминаем прочитанное хорошо, а другой раз не можем вспомнить и строчки уже на следующий день. Так и перманганат калия в окружении ионов OH- ведёт себя по-особенному. У глицерина он забирает электроны «нежнее», никуда не торопясь. Именно поэтому мы можем наблюдать изменение окраски хамелеона.
А что произойдёт, если не добавлять раствор Ca(OH)2?
Когда в растворе присутствует избыток ионов OH-, такой раствор называют щелочным (или говорят, что он имеет щелочную реакцию). Если же, наоборот, в растворе есть избыток ионов H+, такой раствор называют кислым. Почему «наоборот»? Потому что вместе ионы OH- и H+ образуют молекулу воды h3O. А вот если ионы H+ и OH- присутствуют поровну (то есть мы имеем фактически воду), раствор называют нейтральным.
В кислом растворе активный окислитель KMnO4 становится крайне невоспитанным, даже грубым. Он очень быстро отнимает электроны у глицерина (целых 5 за раз!), и марганец превращается из Mn^+7 (в перманганате MnO4-) в Mn2+:
MnO4- + 5e- → Mn2+
Последний (Mn2+) не придаёт воде никакой окраски. Поэтому в кислом растворе марганцовка очень быстро обесцветится, и хамелеон не получится.
Похожая ситуация произойдёт и в случае нейтрального раствора перманганата калия. Только мы «потеряем» не все цвета хамелеона, как в кислом растворе, а только два – зелёный манганат MnO42- получаться не будет, а значит, синее окрашивание тоже исчезнет.
Можно! Хамелеон из хрома (Cr) будет иметь следующую окраску:
оранжевый (бихромат Cr2O72-) → зелёный (Cr3+) → голубой (Cr2+).
Ещё один хамелеон – из ванадия (V):
жёлтый (VO3+) → голубой (VO2+) → зелёный (V3+) → лиловый (V2+).
Вот только заставить растворы соединений хрома или ванадия менять свой цвет так красиво, как это происходит в случае марганца (марганцовки), намного сложнее. Кроме того, придётся постоянно добавлять новые вещества в смесь. Поэтому настоящий хамелеон − такой, что будет менять свой цвет «самостоятельно», − получается только из марганцовки.
Марганец Mn, как и хром Cr и ванадий V, – это переходные металлы – большая группа химических элементов, обладающих целым набором интересных свойств. Одна из особенностей переходных металлов – яркая и разнообразная окраска соединений и их растворов.
Например, из растворов соединений переходных металлов легко получить химическую радугу:

Каждый Охотник Желает Знать, Где Сидит Фазан:
-
Красный (тиоционат железа (III) Fe(SCN)3), железо Fe;
-
Оранжевый (бихромат Cr2O72-), хром Cr;
-
Жёлтый (VO3+), ванадий V;
-
Зелёный (нитрат никеля, Ni(NO3)2), никель Ni;
-
Голубой (сульфат меди, CuSO4), медь Cu;
-
Синий (тетрахлоркобальтат, 2-), кобальт Co;
-
Фиолетовый (перманганат MnO4-), марганец Mn.
Развитие эксперимента
Как изменить хамелеона дальше?
Это интересно
Можно ли обратить реакцию и снова получить фиолетовый раствор?
Некоторые химические реакции могут протекать как в одном направлении, так и в обратном. Такие реакции называют обратимыми и, по сравнению с общим числом химических реакций, их известно не так уж много. Можно обратить реакцию, создав особые условия (например, сильный нагрев реакционной смеси) или добавив какой-то новый реагент. Окисление глицерина перманганатом калия KMnO4 не относится к реакциям такого типа. Более того, в рамках нашего эксперимента обратить эту реакцию невозможно. Поэтому заставить хамелеона менять свой цвет в обратном порядке у нас не получится.
Давайте разберёмся, существует ли способ обратить нашего хамелеона?
Сначала простой вопрос: может ли окисленный глицерин (глицериновая кислота) превратить диоксид марганца MnO2 обратно в фиолетовую марганцовку KMnO4? Нет, не может. Даже если мы будем ему сильно помогать (например, греть раствор). А всё потому, что KMnO4 – сильный окислитель (с этим мы разобрались немного выше), в то время как глицериновая кислота обладает слабыми окислительными свойствами. Слабому окислителю невероятно трудно что-либо противопоставить сильному!
Можно ли превратить MnO2 обратно в KMnO4, используя другие реагенты? Да, можно. Вот только для этого вам придётся работать в настоящей химической лаборатории! Один из лабораторных способов получения KMnO4 – это взаимодействие MnO2 с хлором Cl2 в присутствии избытка гидроксида калия KOH:
2MnO2 + 3Cl2 + 8KOH → 2KMnO4 + 6KCl + 4 h3O
Дома такую реакцию не провести – это и сложно (понадобится специальное оборудование), и небезопасно. Да и сама она будет иметь мало общего с ярким и красивым хамелеоном из нашего опыта.
Раньше почти в каждом доме в аптечке хранились стеклянные пузырьки, наполненные мелкими черными кристалликами – перманганатом калия, в просторечии – марганцовкой. Эта соль известна в фармакологии своими антисептическими свойствами, а также способностью обеззараживать многие яды и очищать воду.
Спектр применения марганцовки в домашних условиях всегда был достаточно широким. Ею обрабатывали раны, лечили язвы, промывали желудок при отравлениях, с помощью слабого раствора очищали для питья воду. И тут внезапно в аптеках перестали продавать этот полезный препарат. Как оказалось, марганцовка запрещена правительством Российской Федерации с 2007 года. В этом году примеру соседа последовала и Украина.
Почему запретили марганцовку? Точнее, ее не запретили, но жестко ограничили продажу в аптеках – теперь перманганат калия можно купить исключительно в государственных фармакологических предприятиях и только при наличии рецепта врача. Оказалось, причин тому несколько, и кроются они в свойствах вещества.
Первой причиной, почему запретили марганцовку, стала ее взрывная способность. Эта соль калия обладает специфическим свойством: при нагреве и даже при комнатной температуре, будучи сильным окислителем, она реагирует на воздействие таких восстановителей, как сахароза, танин, глицерин, а также реакция наблюдается при взаимодействии с порошками активных металлов – кальция, магния, алюминия. При подобных химических реакциях происходит саморазогревание и самовоспламенение вещества (вплоть до взрыва). Вот почему запретили продажу марганцовки. Причиной всему является борьба с террористической деятельностью. То есть знакомый с детства перманганат калия – одно из веществ, используемых при изготовлении самодельных взрывных устройств.
На Украине запрет на продажу этого вещества был введен летом 2013 года. Почему запретили марганцовку в этой стране? Ее причислили к разряду прекурсоров – то есть веществ, используемых в кустарном изготовлении наркотиков. Оказывается, перманганат калия является одним из компонентов для изготовления метамфетамина под названием «первитин», или «винт». В состав этого наркотического средства также входит йод, эфедрин, красный фосфор. Однако гонению подверглась именно марганцовка. В России эта причина также являлась одной из ведущих при внесении описываемого вещества в список запрещенных к продаже препаратов.
 На данный момент в Российской Федерации запрет на продажу марганцовки потихоньку слабеет. При пересмотре списков запрещенных веществ ее частично разрешили к продаже, но в количестве не более 3 миллиграммов. Эксперты в области фармакологии считают подобное решение правильным. Но почему запретили марганцовку? Причины, указанные выше, не изжиты на данный момент, а само по себе такое вещество, как перманганат калия, уже устарело. На смену ему приходят новые поколения антисептиков, которые не задействуют в противозаконных манипуляциях.
На данный момент в Российской Федерации запрет на продажу марганцовки потихоньку слабеет. При пересмотре списков запрещенных веществ ее частично разрешили к продаже, но в количестве не более 3 миллиграммов. Эксперты в области фармакологии считают подобное решение правильным. Но почему запретили марганцовку? Причины, указанные выше, не изжиты на данный момент, а само по себе такое вещество, как перманганат калия, уже устарело. На смену ему приходят новые поколения антисептиков, которые не задействуют в противозаконных манипуляциях.
на протяжении длительного времени считалась лучшим антисептиком. Раствор использовали для заживления ран, лечения некоторых заболеваний и даже применяли в качестве средства укрепления иммунитета у новорожденных детей. За последние несколько лет ситуация изменилась кардинально. Теперь марганцовка – дефицит, а приобрести ее в аптеке довольно сложно.
Причины дефицита
Главной причиной того, что марганцовка стала недоступна для населения – это внесение ее в список «запрещенных препаратов». Произошло это в 2007 году, о чем свидетельствует специальный Указ Правительства РФ. Многие ошибочно полагают, что знаменитый препарат полностью запрещен к производству.
Однако на самом деле это не так. Дело в том, что выпуск марганцовки просто сократили в значительной степени, а продаваться в аптеках она стала исключительно по рецепту. Именно поэтому купить ее на данный момент очень сложно. Большинство населения таким решением не довольно. С давних времен кристаллы перманганата калия разбавляли в воде и использовали для лекарственных целей.
Существует мнение, что причиной запрета свободной продажи марганцовки является специальная программа Правительства, которая рассчитана на борьбу с сомнительными методами самолечения. На самом деле такой вывод не имеет оснований и официально не подтвержден ни в одном источнике. Кроме того, подобной программы просто нет. Некоторые современные специалисты критикуют популярность марганцовки, предлагая заменить ее такими препаратами как, например, антисептический крем «Розамет».
Некоторые аптеки отказались от реализации марганцовки по собственному желанию. Объясняется это решение очень просто. В соответствии с некоторыми изменениями, в значительной степени ужесточились требования хранения этого препарата.
Теперь аптеки должны не только соблюдать новые правила, но и оснащать свои помещения специальным оборудованием. Конечно же, это связано с затратами и выделением отдельной площади для его установки. В большинстве аптечных пунктов такие действия неосуществимы. Например, из-за нехватки площади помещения.
The most common method of application of potassium permanganate – bathing newborns. Now young mothers have to look for an alternative to the famous antiseptics using sea salt or herbs.
Стоит отметить, что взрывные химические реакции могут возникнуть при естественных условиях, например, если не соблюдать условия хранения препарата. Самонагревание гранул может произойти даже при комнатной температуре.
По мнению Правительства РФ взрывной способностью марганцовки могут воспользоваться недоброжелатели в террористических целях. Основанием для такого вывода являются проведенные опыты. Кристаллы перманганата калия взрываются при трении о частички любых металлов.
If you still have stocks of potassium permanganate, pay attention to the expiration date of the drug and never violate the conditions of storage specified on the packaging.
Вторым поводом для ограничения выпуска считается занесение марганцовки в список «прекурсосов». Такие вещества используются для изготовления наркотических веществ в домашних условиях. Самый известный наркотик такого типа — «Винт».
Почему запретили марганцовку
Как разводить марганцовку в ванной? Нам врач сказала должна быть светло розовая вода, у меня получается какая-то коричневая. Может мало марганцовки? Не знаю видно ли по фото
Комментарии
baby-mother.ru
Почему запретили марганцовку и как ее теперь можно приобрести :: SYL.ru
Еще несколько лет назад в каждом доме был пузырек с фиолетовым кристаллами, в народе называемыми марганцовкой. Этот раствор использовался для разных целей. И многие помнят розовую, неприятную на вкус воду, которую приходилось пить при отравлениях или обрабатывать ей раны. Но в последние годы многие люди столкнулись с проблемой: невозможно приобрети этот препарат. И они в недоумении: почему запретили марганцовку? Ведь этот дешевый антисептик часто незаменим в быту и медицине.
Лечебные свойства марганцовки
Научное название этого препарата - перманганат калия. Он является самым популярным антисептиком для наружного и внутреннего применения. Свежий раствор марганцовки обладает окисляющими свойствами и способен убить большинство микробов. Как же применяется марганцовка?
- слабый раствор пьют при отравлениях, диарее и кишечных инфекциях. Такой бледно-розовой водичкой хорошо промывать желудок;
- более концентрированным раствором, до 0,5%, обрабатывают открытые раны, язвы, пролежни и укусы насекомых;
- в педиатрии распространено купание младенцев в ванночке с раствором марганцовки. Это помогает заживить пупочную ранку и обеззараживает воду;
- марганцовкой полощут рот при стоматите и гингивите, лечат больное горло;
- хорошо справляется этот препарат с высыпаниями при герпесе и ветряной оспе;
- ножные ванночки с перманганатом калия помогают при излишней потливости и заживляют мозоли.
Как применяют марганцовку в быту
Раньше это было самым популярным средством для очищения и обеззараживания воды. Эти кристаллы можно, например, добавить в колодец, чтобы обезопасить себя от бактерий.
До сих пор многие садоводы обрабатывают почву и семена перед посадкой слабым раствором марганцовки. Это помогает бороться с вредителями и стимулирует рост растений;
Раствор марганцовки хорошо помогает бороться с неприятными запахами, например, кошачьей мочи.
Может ли быть марганцовка опасной
При разведении препарата нужно внимательно следить, чтобы его кристаллы не попали на кожу и слизистые и полностью растворились в воде. Ведь они могут вызвать сильный ожог и раздражение кожи. Поэтому при приготовлении препарата рекомендуют сначала приготовить более концентрированный раствор, а потом уже его добавлять в воду. Особенно это важно при внутреннем применении марганцовки и при использовании ее для ванночек ребенку. Кроме того, перманганат калия является легковоспламеняющимся веществом, и может произойти взрыв при трении его кристаллов о железо или при нарушении условий хранения.
Почему запретили марганцовку
Этот недорогой и действенный препарат обладает и рядом опасных свойств. Поэтому во многих странах уже давно, а в нашей стране в 2007 году, была марганцовка запрещена. Почему это произошло, станет ясно, если изучить все свойства этого вещества.
1. Соли калия очень нестабильны и при определенных условиях могут воспламеняться, вплоть до взрыва. Это может произойти даже при комнатной температуре и при несоблюдении условий хранения препарата. Этим свойством часто пользуются террористы при изготовлении взрывных устройств. Это одна из причин, почему запретили продажу марганцовки в больших количествах.
2. Кроме того, перманганат калия относится к средствам, которые называются "перекурсоры". Это такие вещества, которые используются для изготовления наркотических средств. И это, скорее всего, главная причина того, почему запретили марганцовку. Во многих странах этот препарат даже относят к наркотикам и могут оштрафовать за его хранение.
Есть ли запрет на продажу марганцовки
Но как ни странно, официально реализация перманганата калия в аптеках не запрещена, а просто ограничена. Те, кто с возмущеньем интересуются, почему запретили продавать марганцовку, получают ответ, что купить ее все-таки можно. Продается препарат по рецепту врача или в небольшом количестве, по 1-2 пакетика в одни руки. Оказывается, на аптеки наложили строгие ограничения и ввели новые правила относительно хранения и продажи препарата. Во многих городах провизоров обязуют вести строгий учет прихода и расхода марганцовки. А сами аптеки должны быть оборудованы специально для безопасного хранения этого взрывоопасного препарата. Поэтому большинство хозяев аптечного бизнеса отказываются продавать такое "неудобное", к тому же недорогое лекарство. Потому приобрести марганцовку можно, но в немногих государственных учреждениях.
Как относятся люди к такому запрету
У некоторых в доме еще остались старые запасы такого нужного препарата. Но те, кто столкнулся с необходимостью купить новую упаковку этого антисептика, выясняют, что марганцовка запрещена. Почему? Люди в недоумении. Ведь существуют еще более опасные препараты и вещества, используемые для приготовления наркотиков. И в то же время они находятся в свободной продаже. Это например, ацетон или средство для прочистки труб "Крот". Для изготовления наркотических средств используется также дистиллированная вода, сахар, кофе и многие другие вещества. Но в ограниченной продаже оказалась только марганцовка. Почему запрещена, причины этого не могут внятно разъяснить ни в одной аптеке. Поэтому люди часто возмущаются. А то, что это пока еще не стало массовым процессом, можно объяснить запасами перманганата калия во многих домах.
Почему запретили марганцовку, можно пока объяснить этими двумя причинами. Но люди понимают, что для тех, кому нужно использовать этот препарат для противозаконных целей, ограничение его продажи не станет препятствием. Ведь можно пройти по многим аптекам, в каждой покупая пакетик марганцовки, и набрать таким образом нужное количество. А вот обычные люди от такого запрета пострадали. Потому что во многих случаях этот недорогой антисептик заменить нечем.
www.syl.ru
Марганцовка: чем полезна

Марганцовокислый калий, калиевая соль марганцовой кислоты или в просторечии – марганцовка – является сильнодействующим окислителем и представляет собой фиолетовые (практически черные) кристаллы с металлическим отливом, которые, при растворении в воде, образуют антисептический раствор различной степени интенсивности цвета (в зависимости от количества вещества от блекло розового до насыщенно малинового).

Именно окисляющая способность марганцовки обеспечивает антисептические и антимикробные качества этой соли. Обеззараживающее действие перманганата калия обусловлено способностью порошка окислять различные органические соединения, в процессе чего выделяется кислород. В годы Великой Отечественной войны кристаллы марганцовки обязательно присутствовали в фельдшерских сумках врачей, медсестер и санитаров. Раствор марганцовокислого калия применялся широко для обработки ран и лечения всевозможных повреждений в госпиталях.
Терапевтические свойства водного раствора марганцовки:
- антимикробное;
- антисептическое;
- противовоспалительное;
- дезинфицирующее;
- обеззараживающее;
- противотоксическое;
- рвотное.
Чем полезна марганцовка для человека
Диапазон применения состава достаточно широк даже, несмотря на доступность новомодных лекарственных препаратов синтетического происхождения. В различных концентрациях (в зависимости от врачебных рекомендаций) раствор марганцовки используют в следующих случаях:
- Промывание ран.
- Ожоги кожных покровов.
- Полоскание ротовой полости, горла при инфекционных заболеваниях слизистой и воспалительных явлениях, в том числе, и при ангине.
- Обработка ожоговых поверхностей ран.
- Смазывание язвенных поверхностей и инфицированных ран.
- Спринцевание при гинекологических и урологических болезнях, в частности, при кольпите и уретрите.
- Промывание желудка при различных отравлениях, спровоцированных попаданием в организм алкалоидов (никотин, морфин и пр.), фосфора, хинина и других, ядовитых для человека веществ.
- Дезинфекция органов ЖКТ при диарее.
- Промывание слизистой глаз при повреждении их насекомыми с ядовитыми свойствами.
- Промывание кожи при попадании на нее ядовитого вещества – анилин.
- Промывание места укуса и примочки при атаке ядовитых змей, тарантула, скорпиона, каракурта.
Разведение марганцовки для различных целей: дозировка и способ применения
Чтобы получить 1% раствор марганцовокислого калия в 99 мл чистой, слегка подогретой (оптимальная температура 35-40°С) воды растворяют 1 гр кристаллов. Не следует для приготовления раствора использовать предметы кухонной утвари из металлов, пластика и т.д. Помните, что перманганат калия – соль, химическое соединение, достаточно активно реагирующее на контакт с различными элементами. Кроме того, красноватые следы марганцовки достаточно трудно удалить с различных поверхностей, например, со стенок эмалированного ковшика или миски. Лучше всего для приготовления раствора воспользоваться стеклянной емкостью нужного объема, например, бутылка из-под сока или банка.
Водный раствор перманганата калия 0,02-0,1% (красный цвет, высокая степень прозрачности) пьют при отравлении (от 0,5 л жидкости), после чего вызывают рвоту для освобождения желудка от содержимого и его детоксикации. Жидкость этой же концентрации используется в урологической и гинекологической практике в виде спринцеваний.
Слабо-розовый раствор марганцовки (0,01-0,1%) употребляют для полоскания ротовой полости и горла при ангине. В случае поноса такой же раствор принимать по 1 стакану состава утром и вечером. После двукратного приема диарея должна прекратиться.
Раствор с процентным содержанием марганцовки 0,1-0,5% (колер красного вина) используют для наружной обработки и дезинфекции ран.
Насыщенно красный раствор (2-5%) готовят для наружной обработки кожных покровов при лечении длительно незаживающих язв и ожогов. Пораженные участки аккуратно смазывают составом. Эту же концентрацию раствора готовят для холодных примочек при свежих ожогах.
Крепкий раствор перманганата калия – 10% применяют для детоксикации и обработки ран, полученных при укусе ядовитой змеи.
Чем полезен перманганат калия для растений
Помимо применения в лечебных целях, марганцовка, благодаря своему обеззараживающему действию, активно используется дачниками в саду и огороде.
Дезинфекция семян марганцовкой
Чаще всего в слабом растворе бледно-розового цвета (0,5%) дезинфицируют посадочный материал (семена и луковицы) большинства цветочных и овощных культур, замачивая их, в зависимости от рекомендаций агрономов, на период от 20 минут до нескольких часов. Помимо обеззараживания такая процедура способствует ускорению прорастания семян, повышая всхожесть посадок, обеспечивает на начальном этапе вегетации потребность в марганце и усиливает иммунитет растений к различным инфекционным заболеваниям.
Польза марганцовки для почвы
Раствор марганцовки (0,2%) используют для обработки почвы как на открытых грядках, так и в теплицах, с целью уничтожения возбудителей многих болезней растений. С этой целью приготовленным раствором проливают землю на грядках или же перед высадкой рассады в каждую лунку вливают по 1 литру такого состава.
Марганцовка в борьбе с заболеваниями садово-огородных культур
3% раствор марганцовки активно используют для борьбы с мучнистой росой на огуречных посадках. Обработку растений проводят каждые 3 дня. Для избавления от мучнистой росы на ягодных кустах (крыжовник, смородина) готовят несколько иной состав: в стандартном ведре воды разводят 50 гр калийной селитры и 3 гр перманганата калия. Обработка растений раствором существенно приостанавливает развитие заболеваний.
Соблюдение осторожности при использовании марганцовки:
Следует понимать, что такое сильнодействующее вещество, при не соблюдении рекомендованных дозировок, может нанести существенный вред здоровью. Высокие концентрации марганцовки при попадании в организм могут вызвать отек слизистых всех органов ЖКТ, ротовой полости и горла, а также усиленную рвоту и расстройство желудка. Поэтому соблюдайте максимальную осторожность при использовании марганцовки. Обязательно храните марганцовокислый калий в недоступном для детей месте.
Имейте в виду, что перманганат калия, при взаимодействии с некоторыми органическими веществами, может образовывать взрывоопасные смеси. Вот почему кристаллы следует сберегать только в стеклянной емкости с плотно притертыми пробками. Приготовленный впрок раствор рекомендуется хранить в затененном месте в бутылях темного стекла, так как при воздействии солнечных лучей и при дневном свете состав быстро разлагается, теряя все свои свойства.
azdorovia.ru
Хамелеон - MEL Chemistry
Что произошло
Почему марганцовка меняет цвет?
Марганцовкой называют раствор перманганата калия KMnO4. Он имеет насыщенный фиолетовый цвет. Однако после добавления глицерина в этот раствор мы наблюдаем достаточно быстрое изменение окраски: пробирка превращается в хамелеона. Что же происходит? В воде KMnO4 распадается на две заряженные частицы:
KMnO4 → K+ + MnO4-

Именно MnO4- отвечает за фиолетовое окрашивание раствора. Частица MnO4- взаимодействует с глицерином. Сначала получается зелёный MnO42-:
MnO4- → MnO42-;
а затем бурый MnO2:
MnO42 → MnO2.
Дополнение
Атом марганца Mn в KMnO4 имеет внушительный положительный заряд (+7). Mn+7 – это сильный окислитель, а значит, он очень хочет заполучить в своё владение электроны (e-). Обычно Mn+7 забирает себе сразу несколько электронов – так сильно он хочет ими «полакомиться». Однако условия нашей реакции подобраны так, чтобы «голодный» марганец не торопился и насыщался электронами постепенно. А глицерин выступает в роли заботливой домохозяйки, подающей марганцу электроны порция за порцией:
MnO4- + e- → MnO42-;
MnO42 + 2e- → MnO2;
MnO2 + 2e- → Mn2+.
Фиолетовый перманганат MnO4- (заряд марганца +7, Mn7+) получает электрон и становится зелёным манганатом MnO42- (заряд марганца +6, Mn6+). Глицерин «кормит» его двумя электронами, и манганат превращается в бурый диоксид марганца MnO2 (Mn4+). Диоксид марганца мог бы взять ещё два электрона и превратиться в бесцветный Mn2+. Однако в условиях нашей реакции MnO2 выпадает в осадок, и этого не происходит.
Реакции, в которых вещества обмениваются электронами, называются окислительно-восстановительными. Жадные до электронов атомы называются окислителями, а те из атомов, которые отдают свои электроны («кормят» окислителей), – восстановителями. В нашем случае марганец – это окислитель, а глицерин – восстановитель.
Кстати, заряды у атомов, (например: +1 у K+, +7 у Mn+7 или -1 у Cl-) химики называют степенями окисления. Подробнее о них вы можете прочитать в описании эксперимента «Исчезающий йод».
Почему раствор поначалу синеет?
Если внимательно следить за хамелеоном, вы заметите, что через несколько секунд после добавления глицерина в раствор он приобретёт синюю окраску. Синий цвет образуется при смешении фиолетового (от перманганата MnO4-) и зелёного (от манганата MnO42-) растворов. Однако он достаточно быстро зеленеет – в растворе становится всё меньше MnO4- и больше MnO42-.
Дополнение
Учёным удалось обнаружить, в какой форме марганец способен окрашивать раствор в синий цвет. Это происходит, когда он образует гипоманганат-ион MnO43-. Здесь марганец находится в степени окисления +5 (Mn+5). Однако MnO43- очень неустойчив, и для его получения необходимы особые условия, поэтому в нашем опыте его увидеть не получится.
Что происходит с глицерином в нашем опыте?
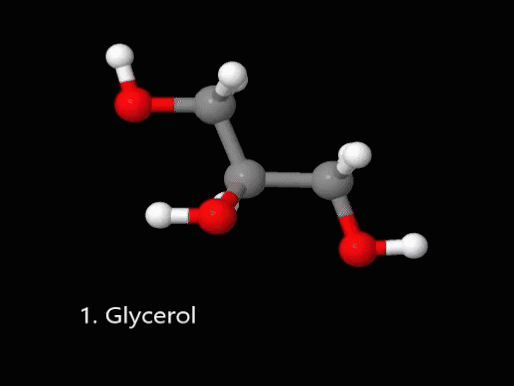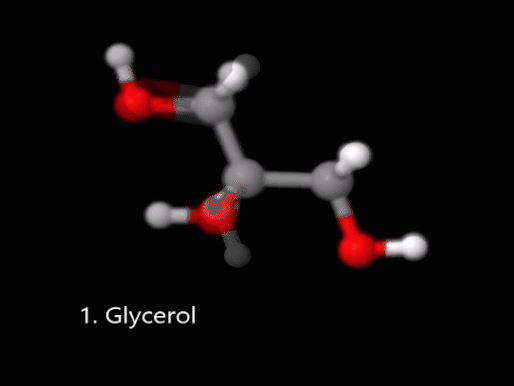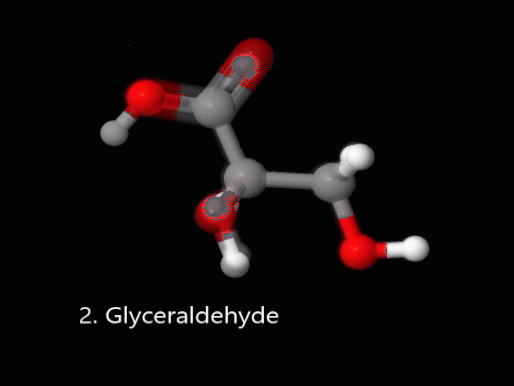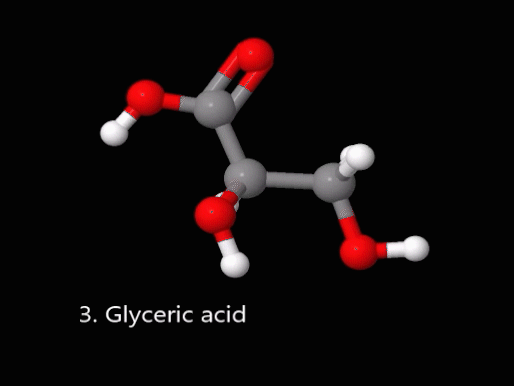
Глицерин взаимодействует с перманганатом калия, отдавая ему свои электроны. Глицерин взят в нашей реакции в большом избытке (его примерно в 10 раз больше, чем перманганата калия KMnO4). Сам глицерин в условиях нашей реакции превращается глицериновый альдегид, а затем − в глицериновую кислоту.
Дополнение
Как мы уже выяснили, глицерин C3H5(OH)3 окисляется перманганатом калия. Глицерин – это весьма сложная органическая молекула, поэтому и реакции с его участием зачастую непросты. Окисление глицерина – сложная реакция, в ходе которой образуется много различных веществ. Многие из них существуют совсем недолго и превращаются в другие, а некоторые можно найти в растворе и после окончания реакции. Такая ситуация характерна для всей органической химии в целом. Обычно те вещества, которых по итогам химической реакции получается больше всего, называют основными продуктами, а остальные – побочными.
В нашем случае основной продукт окисления глицерина перманганатом калия – это глицериновая кислота.
Для чего мы добавляем гидроксид кальция Ca(OH)2 в раствор KMnO4?
В водном растворе гидроксид кальция Ca(OH)2 распадается на три заряженные частицы (ионы):
Ca(OH)2 → Ca2+(раствор) + 2OH-.
В транспорте, магазине, кафе или в школьном классе – везде нас окружают разные люди. И ведём мы себя в таких местах по-разному. Даже если делаем одно и то же дело – например, читаем книгу. В окружении разных людей мы делаем это немного по-разному: где-то медленнее, где-то быстрее, иногда запоминаем прочитанное хорошо, а другой раз не можем вспомнить и строчки уже на следующий день. Так и перманганат калия в окружении ионов OH- ведёт себя по-особенному. У глицерина он забирает электроны «нежнее», никуда не торопясь. Именно поэтому мы можем наблюдать изменение окраски хамелеона.
Дополнение
А что произойдёт, если не добавлять раствор Ca(OH)2?
Когда в растворе присутствует избыток ионов OH-, такой раствор называют щелочным (или говорят, что он имеет щелочную реакцию). Если же, наоборот, в растворе есть избыток ионов H+, такой раствор называют кислым. Почему «наоборот»? Потому что вместе ионы OH- и H+ образуют молекулу воды h3O. А вот если ионы H+ и OH- присутствуют поровну (то есть мы имеем фактически воду), раствор называют нейтральным.
В кислом растворе активный окислитель KMnO4 становится крайне невоспитанным, даже грубым. Он очень быстро отнимает электроны у глицерина (целых 5 за раз!), и марганец превращается из Mn^+7 (в перманганате MnO4-) в Mn2+:
MnO4- + 5e- → Mn2+
Последний (Mn2+) не придаёт воде никакой окраски. Поэтому в кислом растворе марганцовка очень быстро обесцветится, и хамелеон не получится.
Похожая ситуация произойдёт и в случае нейтрального раствора перманганата калия. Только мы «потеряем» не все цвета хамелеона, как в кислом растворе, а только два – зелёный манганат MnO42- получаться не будет, а значит, синее окрашивание тоже исчезнет.
Можно ли сделать хамелеона, используя что-нибудь, кроме KMnO4?
Можно! Хамелеон из хрома (Cr) будет иметь следующую окраску:
оранжевый (бихромат Cr2O72-) → зелёный (Cr3+) → голубой (Cr2+).
Ещё один хамелеон – из ванадия (V):
жёлтый (VO3+) → голубой (VO2+) → зелёный (V3+) → лиловый (V2+).
Вот только заставить растворы соединений хрома или ванадия менять свой цвет так красиво, как это происходит в случае марганца (марганцовки), намного сложнее. Кроме того, придётся постоянно добавлять новые вещества в смесь. Поэтому настоящий хамелеон − такой, что будет менять свой цвет «самостоятельно», − получается только из марганцовки.
Дополнение
Марганец Mn, как и хром Cr и ванадий V, – это переходные металлы – большая группа химических элементов, обладающих целым набором интересных свойств. Одна из особенностей переходных металлов – яркая и разнообразная окраска соединений и их растворов.
Например, из растворов соединений переходных металлов легко получить химическую радугу:

Каждый Охотник Желает Знать, Где Сидит Фазан:
-
Красный (тиоционат железа (III) Fe(SCN)3), железо Fe;
-
Оранжевый (бихромат Cr2O72-), хром Cr;
-
Жёлтый (VO3+), ванадий V;
-
Зелёный (нитрат никеля, Ni(NO3)2), никель Ni;
-
Голубой (сульфат меди, CuSO4), медь Cu;
-
Синий (тетрахлоркобальтат, [CoCl4]2-), кобальт Co;
-
Фиолетовый (перманганат MnO4-), марганец Mn.
Это интересно
Можно ли обратить реакцию и снова получить фиолетовый раствор?
Некоторые химические реакции могут протекать как в одном направлении, так и в обратном. Такие реакции называют обратимыми и, по сравнению с общим числом химических реакций, их известно не так уж много. Можно обратить реакцию, создав особые условия (например, сильный нагрев реакционной смеси) или добавив какой-то новый реагент. Окисление глицерина перманганатом калия KMnO4 не относится к реакциям такого типа. Более того, в рамках нашего эксперимента обратить эту реакцию невозможно. Поэтому заставить хамелеона менять свой цвет в обратном порядке у нас не получится.
Дополнение
Давайте разберёмся, существует ли способ обратить нашего хамелеона?
Сначала простой вопрос: может ли окисленный глицерин (глицериновая кислота) превратить диоксид марганца MnO2 обратно в фиолетовую марганцовку KMnO4? Нет, не может. Даже если мы будем ему сильно помогать (например, греть раствор). А всё потому, что KMnO4 – сильный окислитель (с этим мы разобрались немного выше), в то время как глицериновая кислота обладает слабыми окислительными свойствами. Слабому окислителю невероятно трудно что-либо противопоставить сильному!
Можно ли превратить MnO2 обратно в KMnO4, используя другие реагенты? Да, можно. Вот только для этого вам придётся работать в настоящей химической лаборатории! Один из лабораторных способов получения KMnO4 – это взаимодействие MnO2 с хлором Cl2 в присутствии избытка гидроксида калия KOH:
2MnO2 + 3Cl2 + 8KOH → 2KMnO4 + 6KCl + 4 h3O
Дома такую реакцию не провести – это и сложно (понадобится специальное оборудование), и небезопасно. Да и сама она будет иметь мало общего с ярким и красивым хамелеоном из нашего опыта.
Какие ещё цвета могут быть у соединений марганца?
Где используют окрашенные соединения марганца?
Роза инков
melscience.com
применение и меры предосторожности :: SYL.ru
Каждый человек в своей жизни хотя бы раз слышал о таком средстве, как марганцовка. Применение его широко распространено в медицине. Это отличный противомикробный препарат для наружного использования, так как он имеет обеззараживающее свойство. Данное вещество имеет официальное название – «марганцевокислый калий» и используется как антисептик. Производители рассматриваемого средства выпускают его в виде порошка (очень мелкие кристаллы), а срок годности его не ограничен.
Как действует марган0цовка?
Если раствор марганцовки сильно концентрированный, у него темно-фиолетовая окраска, но при маленькой дозе препарата в воде она становится светло–розовой. Пока раствор перманганата калия свежий, он обладает очень сильной окисляющей активностью. За эти свойства его очень ценят в медицине. Раствор, нанесённый на поверхность тела, способен уничтожить патогенные возбудители, которые есть на ней. Однако стоит знать: на это способен только лишь свежеприготовленный раствор марганцовки. Как определить его «возраст»? Свежий и старый растворы отличаются по цвету. Если вода имеет буро–красный или буро–коричневый оттенки, значит такое лекарство уже стало непригодным. Свежий раствор окрашен в малиновый цвет. Стоит отметить, что только его рекомендуют использовать для наружного применения.
Приготовление раствора перманганата калия
Не все знают, что кристаллы растворяются в воде, поэтому есть риск получить ожог слизистой желудка или кожи от нерастворенных кристаллов. Чтобы избежать таких осложнений, сначала приготавливают концентрированный раствор. Только потом его используют, чтобы добавить в воду, которую пьют. Важно знать, что марганцовку разводят в тёплой или горячей воде, в холодной она не растворится полностью. Если лекарство готовится в водопроводной воде, то срок его хранения составляет около суток, а вот дистиллированная жидкость увеличивает время его пригодности до шести месяцев. Важно помнить, что раствор хранят в банках с затемнённым стеклом, вдали от солнечных лучей.
Как избавиться от пятен?
Стоит отметить, что марганцовка, применение которой во многих случаях оставляет после себя тёмные пятна на коже или одежде, часто называется «спасительницей». Но вот избавиться от пятен нелегко: простые моющие средства не помогут. Что же тогда делать? Ответ прост: вам поможет щавелевая или аскорбиновая кислота. Если применить одну из них, то вы затратите минимум усилий. Весь секрет кроется в химической реакции, которая происходит при контакте веществ. Очень быстро пятна исчезнут сами собой.
Марганцовка: применение
Кристаллы марганцовки и концентрированный раствор можно применять для прижигания бородавок и мозолей. Разведенный препарат нашел широкое применение. Его используют для промывки ран ожоговой и язвенной этиологии. Также лекарство применяют для проведения таких процедур: полоскание гортани и ротовой полости, спринцевание влагалища и обработка полового члена у мужчин, промывание желудка при отравлении лекарствами и др. веществами (для этого используют свежеприготовленный раствор марганцовки с концентрацией 0,01 – 0,5 %). Нередко спасает марганцовка при отравлении ядовитыми веществами или наркотиками. Всегда, когда возникает необходимость в применении препарата, необходимо знать простое правило. Так как антисептическое действие раствора по времени коротко, то и микробы исчезают лишь на время обработки раны. Другими словами, для более длительного воздействия он непригоден.
Марганцовка: применение в домашних условиях
Очень часто молодые мамы применяют марганцовку при купании новорождённых детей. Эта процедура выполняется очень осторожно! Во-первых, в воду, в которой купают малыша, ни в коем случае нельзя добавлять марганцовку в виде нерастворенных кристаллов. Во-вторых, сначала приготавливают раствор, удаляют кристаллы нерастворенные, а только потом добавляют в ванну с водой немного полученной жидкости. Важно помнить, что раствор должен быть слабой концентрации, чтобы не подсушить кожу малыша. Марганцевокислый калий - отличный борец с конъюнктивитом. Лечение проводят путём промывания глаз очень слабым раствором. Также он помогает справиться с ангиной и стоматитом. Просто промывают ротовую полость слабым раствором. Однако марганцовка не только помогает при заболеваниях глаз или горла, но и спасает от такой распространённой проблемы, как понос. Как рекомендуют медики в таких случаях, нужно два раза в день выпивать по одному стакану слабого раствора марганцовки. Это действительно способно позволить забыть о расстройстве желудка на долгое время. Есть люди, которые страдают от вросшего ногтя. И тут марганцовка приходит на помощь. Достаточно принимать ванночки, наполненные слабым раствором. Однако лечение рассматриваемым препаратом поможет лишь на начальной стадии болезни. Чтобы не запустить недуг, его нужно вовремя лечить. Итак, если почувствуете дискомфорт в области пальца, то немедленно начинайте применение указанного способа терапии. Ведь если вы запустите процесс, то может понадобиться хирургическое вмешательство. Марганцовка при молочнице широко применялась года два назад. Однако сейчас научно подтвердили, что такое лечение наносит вред микрофлоре влагалища. Также многие огородники применяют данное вещество для борьбы с различными вредителями.
Осложнения и противопоказания
Осложнения могут возникнуть при нанесении раствора перманганата калия высокой концентрации на поверхность тела или же когда кристаллы не растворились до конца. Это все может привести к раздражению кожи или вызвать ее ожог. Раствор марганцовки используют очень осторожно! При соприкосновении кристаллов препарата с очень быстро окисляющими веществами органического происхождения может возникнуть пожар или даже взрыв. Поэтому данное средство считают огнеопасным.
www.syl.ru
Большой вопрос: "Почему запретили марганцовку?"
Раньше почти в каждом доме в аптечке хранились стеклянные пузырьки, наполненные мелкими черными кристалликами – перманганатом калия, в просторечии – марганцовкой. Эта соль известна в фармакологии своими антисептическими свойствами, а также способностью обеззараживать многие яды и очищать воду.
Спектр применения марганцовки в домашних условиях всегда был достаточно широким. Ею обрабатывали раны, лечили язвы, промывали желудок при отравлениях, с помощью слабого раствора очищали для питья воду. И тут внезапно в аптеках перестали продавать этот полезный препарат. Как оказалось, марганцовка запрещена правительством Российской Федерации с 2007 года. В этом году примеру соседа последовала и Украина.
 Почему запретили марганцовку? Точнее, ее не запретили, но жестко ограничили продажу в аптеках – теперь перманганат калия можно купить исключительно в государственных фармакологических предприятиях и только при наличии рецепта врача. Оказалось, причин тому несколько, и кроются они в свойствах вещества.
Почему запретили марганцовку? Точнее, ее не запретили, но жестко ограничили продажу в аптеках – теперь перманганат калия можно купить исключительно в государственных фармакологических предприятиях и только при наличии рецепта врача. Оказалось, причин тому несколько, и кроются они в свойствах вещества.
Первой причиной, почему запретили марганцовку, стала ее взрывная способность. Эта соль калия обладает специфическим свойством: при нагреве и даже при комнатной температуре, будучи сильным окислителем, она реагирует на воздействие таких восстановителей, как сахароза, танин, глицерин, а также реакция наблюдается при взаимодействии с порошками активных металлов – кальция, магния, алюминия. При подобных химических реакциях происходит саморазогревание и самовоспламенение вещества (вплоть до взрыва). Вот почему запретили продажу марганцовки. Причиной всему является борьба с террористической деятельностью. То есть знакомый с детства перманганат калия – одно из веществ, используемых при изготовлении самодельных взрывных устройств.
 На Украине запрет на продажу этого вещества был введен летом 2013 года. Почему запретили марганцовку в этой стране? Ее причислили к разряду прекурсоров – то есть веществ, используемых в кустарном изготовлении наркотиков. Оказывается, перманганат калия является одним из компонентов для изготовления метамфетамина под названием "первитин", или "винт". В состав этого наркотического средства также входит йод, эфедрин, красный фосфор. Однако гонению подверглась именно марганцовка. В России эта причина также являлась одной из ведущих при внесении описываемого вещества в список запрещенных к продаже препаратов.
На Украине запрет на продажу этого вещества был введен летом 2013 года. Почему запретили марганцовку в этой стране? Ее причислили к разряду прекурсоров – то есть веществ, используемых в кустарном изготовлении наркотиков. Оказывается, перманганат калия является одним из компонентов для изготовления метамфетамина под названием "первитин", или "винт". В состав этого наркотического средства также входит йод, эфедрин, красный фосфор. Однако гонению подверглась именно марганцовка. В России эта причина также являлась одной из ведущих при внесении описываемого вещества в список запрещенных к продаже препаратов.
 На данный момент в Российской Федерации запрет на продажу марганцовки потихоньку слабеет. При пересмотре списков запрещенных веществ ее частично разрешили к продаже, но в количестве не более 3 миллиграммов. Эксперты в области фармакологии считают подобное решение правильным. Но почему запретили марганцовку? Причины, указанные выше, не изжиты на данный момент, а само по себе такое вещество, как перманганат калия, уже устарело. На смену ему приходят новые поколения антисептиков, которые не задействуют в противозаконных манипуляциях.
На данный момент в Российской Федерации запрет на продажу марганцовки потихоньку слабеет. При пересмотре списков запрещенных веществ ее частично разрешили к продаже, но в количестве не более 3 миллиграммов. Эксперты в области фармакологии считают подобное решение правильным. Но почему запретили марганцовку? Причины, указанные выше, не изжиты на данный момент, а само по себе такое вещество, как перманганат калия, уже устарело. На смену ему приходят новые поколения антисептиков, которые не задействуют в противозаконных манипуляциях.
fb.ru